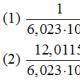Секции на сайта
Избор на редакторите:
- Сензационно откритие: многоизмерна вселена, открита в мозъка ни
- Комбиниран мост Øresund между Дания и Швеция Границата между Дания и Швеция
- "три столици" на Литва Къде да отида в Литва
- GCD резюме за рисуване - Ракета в космоса
- GCD резюме за рисуване - Ракета в космоса
- Марина Бородицкая: „Литературата е бомбоубежище Въпроси, от които да избирате
- Треньор за Watch Dogs - неуязвимост, безкрайни боеприпаси, точки за надграждане, опит и много други
- Тъжно ускорение: морското равнище се покачва дори по -бързо, отколкото се смяташе досега
- Коля ще го направи. Отиваме на училище. Какво да облека за момиче
- Военни паради по целия свят
Реклама
| Устройство, което измерва количеството топлина. Принципът на работа на топломера. Фактори, влияещи върху крайния резултат от измерването |
|
Необходимостта от бързо определяне на консумацията на топлина и топлинните загуби стана особено остра през последните години, когато търсенето за пестене на горива и енергийни ресурси излезе на преден план. Консумацията на топлина се измерва с помощта топломери ... В този случай проблемът се решава в съответствие с алгоритъма: Q = V T C T t (T 1 -T 2), MJ, където: В- количеството топлина, отделяно от охлаждащата течност по време на T; V T- обемен дебит на охлаждащата течност (вода), m 3 / s; Т 1;Т 2- температура на охлаждащата течност на входа и изхода на потребителя, 0 С; C T- специфичен топлинен капацитет на охлаждащата течност, MJ / m 3. В най -простия случай веригата на топломера трябва да съдържа сензор за потока на охлаждащата течност (водомер), два температурни сензора и изчислителна единица, която реализира горния алгоритъм (фиг. 5.7). В промишлените системи са необходими по -сложни схеми на топломери, които отчитат промяната в енталпията на охлаждащата течност и консумацията на топлина за подаване на топла вода. Индивидуални топломери, широко разпространени в редица европейски страни, оценяват консумацията на топлина от отделни потребители, например радиатори за централно отопление (виж фиг. 5.8). Те съдържат чувствителен елемент - градуирана стъклена тръба, пълна с тетралин. Систематичното му загряване води до изпаряване на течността, по което се преценява консумацията на топлина. Изчисляването на консумацията на топлина се извършва с помощта на компютър, в базата данни на който предварително са въведени характеристиките на всеки радиатор. Ориз. 5.7. Схема на най-простия топломер: 1-захранващ (прав) тръбопровод; Тръбопровод с 2 изхода (връщане); 3-водомер; 4-температурен сензор за охлаждащата течност; 5-температурен сензор на използвания топлоносител.
Ориз. 5.8. Индивидуален топломер на радиатора за централно отопление. Има три основни начина за управление на процесите на топлоснабдяване и захранване - ръчен, автоматичен и полуавтоматичен. За тяхното изпълнение се използват различни устройства и устройства. Най -често срещаните са: ръчни кранове, вентили, ключове, ключове и регулатори с различни параметри. Нека да разгледаме някои от тях. Соленоидни клапани - това са устройства, в които движението на клапана се осигурява от електромагнит (фиг. 5.9). Електромагнитният клапан по правило осигурява две позиции - отворена и затворена. Клапанът се отваря, когато има управляващо напрежение от управляващата верига. При негово отсъствие клапанът се задържа затворен от действието на пружината.
Ориз. 5.9. Соленоиден клапан: 1-тръбопровод; 2-клапан; 3-подвижна сърцевина; 4-соленоид; 5-пружинен. Електромеханичен кран (вентил) съдържа кран или вентил като работно тяло. Работното тяло се задвижва от електродвигател, зъбна рейка, зъбни механизми или червячна предавка. За увеличаване на усилието и намаляване на скоростта на крана се използва редуктор (фиг. 5.10). Чрез промяна на полярността на захранващото напрежение, подадено към DC двигателя, вентилът може да бъде затворен или отворен. Ако се използва променливотоков двигател, той трябва да се обърне обратно чрез превключване на намотките. Електромеханичните устройства ви позволяват плавно да променяте положението на работния орган (вентил, кран) от напълно отворен до напълно затворен. Това осигурява плавно регулиране на дебита от υ w = 0преди υ w = υ макс . .
Ориз. 5.10. Електромеханичен клапан: 1-тръбопровод; 2-клапан; 3-стелажен механизъм; 4-степенна; 5-електродвигател. Електрически помпи позволяват движението на течности и газове през тръбопроводи от зони с ниско статично налягане до зони с по -високо налягане. Ефективно е използването на регулируеми (например честотно регулиране) електрически задвижвания, които подобряват работата на системата за управление и осигуряват значителни икономии на енергия. Автоматични регулатори - това са устройства, които осигуряват поддържането на параметъра на обекта на постоянно ниво или промяната му съгласно даден закон. Автоматичният регулатор трябва да съдържа: чувствителен елемент или сензор с регулируем параметър; регулаторен орган; устройство за настройка, което определя необходимата стойност на параметъра. Пример за такова устройство е автоматичен термостат, монтиран пред отоплителните устройства на отоплителната система (фиг. 5.11). Работи по следния начин. Клапанът, припокриващ тръбопровода, е механично свързан към запечатан хармонично чувствителен елемент-термичен сензор, чиято вътрешност е изпълнена с чувствителна към температурата маса, която може да се разширява с повишаване на температурата. С повишаване на температурата на въздуха в помещението, температурният сензор се разширява и затваря тръбопровода, което ограничава потока на охлаждащата течност в радиатора. Необходимата стайна температура може да се регулира ръчно чрез завъртане на защитната капачка с пружина. Измервател на енергия на частици. Колегиален YouTube1 / 5 ✪ ИЗПОЛЗВАНЕ 2014 Физика: A9 - алуминиев цилиндър беше потопен в калориметър със студена вода Физика 8 клас. Количество топлина. Единици за измерване на количеството топлина ✪ Физика Калориметърът съдържа вода с маса mw = 2 kg, чиято температура е 30 ° C. В калориметъра Exper Експерименти на Джоул ✪ Физика | Подготовка за Олимпиадата 2017 | Проблемът "Калориметърът е запален" СубтитриСъвременни калориметриСъвременните калориметри работят в температурния диапазон от 0,1 до 3500 и могат да измерват количеството топлина с точност от 0,01-10%. Дизайнът на калориметрите е много разнообразен и се определя от естеството и продължителността на изследвания процес, диапазона от температури, при които се извършват измервания, количеството на измерената топлина и необходимата точност. Видове калориметриКалориметър, предназначен за измерване на общото количество топлина В, който се откроява в процеса от началото до завършването му, се нарича интегратор калориметър Калориметър за измерване на топлинната мощност (скорост на отделяне на топлина) Lи неговите промени на различни етапи от процеса - силометърили осцилоскоп калориметър... Според дизайна на калориметричната система и метода на измерване се разграничават течни и масивни калориметри, единични и двойни (диференциални). Течен калориметър-интеграторТечен калориметър-интегратор с променлива температура с изотермична обвивка се използва за измерване на топлините на разтваряне и топлините на химичните реакции. Състои се от съд с течност (обикновено вода), който съдържа: камера за провеждане на изследвания процес ("калориметрична бомба"), бъркалка, нагревател и термометър. Топлината, отделена в камерата, след това се разпределя между камерата, течността и други части на калориметъра, чиято съвкупност се нарича калориметрична система на инструмента. В течните калориметри изотермичната температура на черупката се поддържа постоянна. При определяне на топлината химическа реакцияНай -големите трудности често са свързани не с отчитане на страничните процеси, а с определяне на пълнотата на реакцията и с необходимостта да се вземат предвид няколко реакции. Калориметрични измерванияПромяната на състоянието (например температурата) на калориметричната система дава възможност за измерване на количеството топлина, въведена в калориметъра. Нагряването на калориметричната система се записва с термометър. Преди да се направят измервания, калориметърът се калибрира - промяната в температурата на калориметричната система се определя, когато към нея се подаде известно количество топлина (от калориметъра на нагревателя или в резултат на химична реакция с известно количество от стандартно вещество в камерата). В резултат на калибрирането се получава топлинната стойност на калориметъра, тоест коефициентът, с който температурната промяна на калориметъра, измерена с термометъра, трябва да се умножи, за да се определи количеството топлина, въведена в него. Топлинната стойност на такъв калориметър е топлинният капацитет (с) на калориметричната система. Определяне на неизвестна топлинна стойност или друга химична реакция Все свежда до измерване на температурната промяна Δ Tкалориметричната система, причинена от изследвания процес: Q = cΔ T... Обикновено стойността Все отнасят до масата на веществото в калориметровата камера. Странични процеси при калориметрични измерванияКалориметричните измервания дават възможност директно да се определи само сумата от топлините на разглеждания процес и различни странични процеси, като смесване, изпаряване на вода, счупване на ампула с вещество и др. Топлината на страничните процеси трябва да се определи емпирично или чрез изчисление и изключени от крайния резултат. Един от неизбежните странични процеси е топлообменът на калориметъра с заобикаляща средачрез радиация и топлопроводимост. За да се вземат предвид страничните процеси и най -вече преносът на топлина, калориметричната система е заобиколена от черупка, чиято температура се контролира. Изотермичен интегратор калориметърВ калориметър -интегратор от друг тип - изотермичен (постоянна температура), въведената топлина не променя температурата на калориметричната система, но причинява промяна в агрегатното състояние на тялото, което е част от тази система (например, топене на лед в ледовия калориметър Bunsen). Количеството на въведената топлина се изчислява в този случай от масата на веществото, което е променило агрегатното състояние (например масата на разтопения лед, която може да бъде измерена чрез промяната в обема на сместа от лед и вода ) и топлината на фазовия преход. Масивен интегратор калориметърНай -често се използва масивен интеграторен калориметър за определяне на енталпията на веществата при високи температури (до 2500 ° C). Калориметричната система от този тип калориметри е метален блок (обикновено меден или алуминиев) с вдлъбнатини за реакционния съд, термометър и нагревател. Енталпията на дадено вещество се изчислява като произведение на топлинната стойност на калориметъра от разликата в повишаването на температурата на блока, измерена след пускане на ампула с определено количество вещество в гнездото си, и след това празна ампула, загрята до същата температура. Дебитни лабиринтни калориметриТоплинният капацитет на газове, а понякога и течности, се определя в т.нар. дебитни лабиринтни калориметри - въз основа на температурната разлика на входа и изхода на неподвижен поток от течност или газ, силата на този поток и топлината от Джоул, отделяна от електрическия нагревател на калориметъра. Калориметър - Измервател на мощностКалориметър, работещ като електромер, за разлика от интегриращия калориметър, трябва да има значителен топлообмен, така че количеството топлина, въведено в него, да бъде бързо отстранено и състоянието на калориметъра се определя от моментната стойност на мощността на термичен процес. Топлинната мощност на процеса се намира от топлообмена на калориметъра с обвивката. Такива калориметри, разработени от френския физик Е. Калвет, са метален блок с канали, в които са поставени цилиндрични клетки. Изследваният процес се провежда в клетката; металният блок играе ролята на черупка (температурата му се поддържа постоянна с точност 10−5 -10 −6 K). Температурната разлика между клетката и блока се измерва с термопила с до 1000 кръстовища. Топлообменът на клетката и ЕМП на термопилата са пропорционални на малката температурна разлика, която възниква между блока и клетката, когато топлината се освобождава или абсорбира в нея. Най -често в блока се поставят две клетки, които работят като диференциален калориметър: термопилите на всяка клетка имат еднакъв брой кръстовища и поради това разликата в техния ЕМП дава възможност директно да се определи разликата в мощността на топлинните потоци навлизане в клетките. Този метод на измерване елиминира изкривяването на измерената стойност чрез случайни колебания в температурата на блока. Обикновено на всяка клетка се монтират по две термопили: едната позволява да се компенсира топлинната мощност на изследвания процес въз основа на ефекта на Пелтие, а другата (индикатор) служи за измерване на некомпенсираната част от топлинния поток. В този случай устройството работи като калориметър с диференциална компенсация.При стайна температура такива калориметри измерват топлинната мощност на процесите с точност от 1 μW. Имена на калориметриОбщите имена на калориметри - „за химична реакция“, „бомба“, „изотермичен“, „лед“, „нискотемпературна“ - имат исторически произход и посочват главно метода и областта на използване на калориметъра, като не са нито пълна, нито сравнителна характеристика. Обща класификация на калориметритеОбща класификация на калориметрите може да бъде изградена въз основа на разглеждане на три основни променливи, които определят техниката на измерване: температурата на калориметричната система Т в; температура на черупката Да сезаобикаляща калориметричната система; количеството топлина Lосвободени в калориметъра за единица време (топлинна мощност). Калориметри с константи Т ви Да сенаречен изотермичен; с Т в = Да се- адиабатни; калориметър с постоянна температура Т в - Да се, се нарича калориметър с постоянен топлообмен; за калориметър с изоперибол (наричан още изотермичен калориметър с черупка) е постоянен Да се, а Т ве функция на топлинната мощност L. Фактори, влияещи върху крайния резултат от измерванетоВажен фактор, влияещ върху крайния резултат от измерването, е надеждната работа на автоматичните регулатори на температурата за изотермични или адиабатни черупки. В адиабатичен калориметър температурата на черупката се контролира така, че винаги да е близка до променящата се температура на калориметричната система. Адиабатната обвивка, лек метален екран, оборудван с нагревател, намалява топлопредаването толкова много, че температурата на калориметъра се променя само с няколко десетки хилядни от градус / мин. Това често прави възможно намаляването на топлопредаването по време на калориметричния експеримент до незначителна стойност, която може да се пренебрегне. Ако е необходимо, в резултатите от директните измервания се въвежда корекция за пренос на топлина, чийто метод на изчисление се основава на закона на Нютон за топлопреминаване - пропорционалността на топлинния поток между калориметъра и обвивката на тяхната температурна разлика, ако това разликата е малка (до 3-4 ° C). За калориметър с изотермична обвивка топлините на химичната реакция могат да се определят с грешка до 0,01%. Ако размерите на калориметъра са малки, температурата му се променя с повече от 2–3 ° C и изследваният процес е дълъг, тогава с изотермична обвивка корекцията за пренос на топлина може да бъде 15–20% от измерената стойност и значително ограничават точността на измерването. В тези случаи е по -целесъобразно да се използва адиабатна обвивка. С помощта на адиабатичен калориметър топлинният капацитет на твърди и течни вещества се определя в диапазона от 0,1 до 1000 К. При стайна и по -ниска температура адиабатичен калориметър, защитен с вакуумна обвивка, се потапя в колба на Дюар, пълна с течен хелий, водород или азот. При повишени температури (над 100 ° C) калориметърът се поставя в термостатирана електрическа фурна. "Конвекция" - Процесът на смесване. Термогравитационна конвекция. Конвекция. Естествена конвекция. Видове конвекция поради външния вид. Какво е конвекция Има два вида конвекция. Видове конвекция. Движението на материята се дължи на действието на някои външни сили. Топлообмен. Принудителна конвекция. Атмосферни явления. "Химическа технология на горивото" - Горива за РДВ. Газове. Цетаново число. Бензини. Изчислено определяне на централната част. Октаново число на различни групи въглеводороди. Парафини и церезини. Изчислителни методи. Тенденцията на моторните горива да детонират. Дизелови горива. Запалимост. Газова турбина и котелно гориво. Теоретична основахимическа технология. "Вътрешна енергия" - Материали с лоша топлопроводимост. Вътрешна енергия. Частици материя. Енергията също се увеличава с деформация. Отопляеми тела. Вътрешната енергия намалява. Загряване на лъжица във вряща вода. Видове топлопреминаване. Метали. Какво е агрегатното състояние на тялото. Механична енергия. "Изчисляване на количеството топлина" - Определяне на количеството топлина. Количество топлина. Разрешаване на проблеми. Формула за изчисляване на количеството топлина. Повторение. Изчисляване на количеството топлина. Изучаване на нов материал. Решете проблемите. Реши задачата. Колко топлина е необходима за отопление. Разлика. Какво се показва от специфичната топлина на веществото. "Методи за пренос на топлина" - Нагряване на течността. Преса за хартия. Топка. Топлопроводимост. Отопление на вода. Керосинова лампа. Пригответе лед във фризера. Дупки. Методи за пренос на топлина. Защо се чувстваме готини, когато се раздуваме. Прозоречно стъкло. Видове пренос на топлина в термос. Огън в ситото. Видове топлопреминаване. Радиация. „Количество топлина“ - Q– топлина, получена от тялото. Топлообмен. Историята на възникването на понятия. Какво е количеството топлина. Количество топлина. Устройство за измерване на количеството топлина. Съвременни калориметри. Дж. Джоул, английски физик, изследвал топлинни явления. Калориметър. Адиабатичен калориметър с висока точност. Общо има 30 презентации В тази статия ще отговорим на въпроса: "Какво е калориметър?" Определяме основни характеристикина този механизъм, неговия принцип на действие и приложения, функционалност и измервателни стойности. Ще обърнем внимание и на класификацията и описанието на някои специфични видове. ВъведениеОтговаряйки на въпроса какво е калориметър, в общи линии той може да бъде описан като устройство, чрез което се измерва количеството топлина, което се отделя или абсорбира в хода на физични, химични или биологични процеси. Въвеждането на нова терминологична единица "калориметър" е предложено през 1780 г. от П. Лаплас и А. Лавоазие. Подобно устройство се използва и в секцията за ядрена физика, която изучава елементарни частици, и се нарича йонизационен калориметър. Функцията на това устройство обаче е да измерва енергийния потенциал на частиците.
Съвременен механизъмОпределянето на топлинния капацитет от модерен калориметър дава възможност да се фиксира изследваната стойност с точност от десет до стотна част от процента. Диапазонът, в който това устройство може да работи, варира от 0,1 до 3500 Kelvin. Видът на калориметърното устройство е много разнообразен. Тя може да бъде определена от естеството на процеса, който се изучава, както и от неговата продължителност. Друг важен параметър за определяне на типа на механизма е температурният диапазон, в който се извършват измерванията, както и количеството на измерената стойност на топлината. Определянето на енергийния еквивалент с калориметър може да покаже на субекта количеството тяло, което се отделя при изгарянето на горивния ресурс. Това може да стане благодарение на израза Q = C∆T, в който C е показател за термичния (енергиен) еквивалент. Задайте параметрите за дефиниция, като калибрирате инструмента. Друга стойност на ∆T е функция на известния изход от калориметъра. Разпределение по видНевъзможно е да се отговори на въпроса какво е калориметър, без да се запознаете с неговите видове. Един от най -често срещаните представители на такива устройства е интеграторният калориметър. Той има за цел да определи общото количество топлина Q, което се отделя в началото на реакцията и нейния край. Друг добре известен калориметър е устройство за измерване на мощността на топлината, тоест скоростта, с която се отделя топлина - L. И те също могат да бъдат разделени според дизайна на механизма и методологията на измерване, подход. Различават се и калориметри от течен и масивен тип. Има и единични и диференциални устройства. Измерване на топлината
Какво е калориметър във физиката? Определението казва, че това е устройство за измерване на количеството генерирана топлина. В този случай топлината, отделена в хода на химическа реакция, може да бъде разпозната само благодарение на течен калориметър-интегратор. Дизайнът е представен под формата на съд, напълнен с течност (обикновено вода). Съдържа камера за провеждане на експеримент ("калориметрична бомба"), бъркалка, термометър и нагревателно устройство. Измервания на калориметрична система
Корекциите на естествения ход на генериране на топлина в системата могат да бъдат открити, когато някое от нейните състояния се промени. Те от своя страна се определят чрез анализ на количеството топлина, което се вкарва в устройството. Константата на калориметъра се определя преди началото на измервателната работа и се сравнява с зададената и коригираната стойност. Устройствата са калибрирани, поради което се определя коефициентът. Тя трябва да се умножи с изменението на температурата на устройството, измерено с термометъра. Наличието на странични ефектиВсъщност калориметричните данни показват директно само общия брой топлини, които се изследват в процеса. Можете също така да разберете за наличието на страничен процес (или процеси), който може да причини явлението смесване, изпаряване на течността, както и счупване на ампула с вещества и т.н. Определянето на константата на калориметъра позволява на човек да получи достъп до сравнение на индикатори за промени на фона на нещо. С негова помощ се анализира информацията. Топлината на странични серии процеси трябва да се определи, като се използва опит или изчисление, изключено от резултатите от изследването. Пример за страничен ефект е неизбежният топлообмен между калориметъра и околното пространство и материята. Изотермични наблюденияСъществува интегриращ калориметър от изотермичен тип, който позволява да се въведат промени в агрегатните състояния на телата, които формират основната част на системата. Пример за това е топенето на маса лед ледена камераБунзен калориметър. Можете да разберете промяната в топлината, която влияе върху агрегатното състояние, но не предизвиква промяна в температурата, ако изчислите масата на веществото и количеството топлина, което би било необходимо за това. За да се определи специфичната топлина на калориметър, е необходимо да се знае, че тя е числено равна на количеството топлина, което се изразходва за нагряване на единица маса материя. Неговата единица е J / kg▪K. Важно е да запомните, че специфичният топлинен капацитет е двусмислена характеристика. Съществува връзка между условията за осъществяване на топлопредаване и стойността на работата, която съпътства този процес. Масивен тип
За да се определи стойността на енталпията на вещество при температури до 2500 градуса по Целзий, се използват масивни интегратори. Масата на този тип калориметри може да варира в зависимост от теглото на измерваното вещество, тъй като структурата се състои от метали. Всъщност това е блок с редица вдлъбнатини за кораби. При тях протичат реакции, предназначени за нагревателно устройство и / или термометър. Продуктът на топлинната стойност, измерена с калориметъра, и разликата в повишаването на температурата в блока ни показва енталпията на веществата (а). ПотокМожете да определите топлинния капацитет на газ или течност с помощта на дебитен лабиринт калориметър. Той записва температурната разлика, която влиза и излиза от неподвижните потоци на изпитваното вещество. Той също така определя силата на такъв поток и силата на топлината, която се отделя от електрическия нагревател, в джаули. СилометърОтговаряйки на въпроса какво е калориметър, ще бъде важно да споменем предназначението на това устройство за определяне на мощността. Такова устройство, за разлика от интегратора, трябва да бъде снабдено със значителен капацитет за топлообмен. Това е необходимо, за да може да премахне количеството топлина, което се внася в него. От това следва, че състоянието на калориметъра е мигновено. Топлинната стойност на мощността на процеса се установява чрез използването на калориметри с обвивка. Изобретението е направено от физик от Франция Е. Калвет. Първоначално механизмът е представен под формата на метален блок, снабден с канали. Върху тях бяха поставени специални цилиндрични клетки, предназначени за провеждане на изследвания процес. Металът, използван при изграждането на камерата, е обвивката. Температурата му трябва да се поддържа на постоянно ниво с точност от пет до шест Келвина.
Измерването на разликата между температурата на клетката и блока се извършва с помощта на термопила с до хиляда сраствания. Скоростта на пренос на топлина в ЕМП и клетката е пропорционална на малката разлика в температурата, която възниква между компоненти като блок и клетка. В този случай топлината трябва да се отделя или абсорбира в самата клетка. Много често в такива блокове има няколко клетки, които ще работят различно. Име и класификацияОбщите имена за калориметри са:
Всички те имат данни за исторически произход... Обикновено дължат името си на района, в който ще бъдат използвани. Тези имена обаче не са свързани със сравнително или пълно описание. Общ изглед на класификацията на калориметрите се изгражда, като се използва като основа разглеждане на едно от трите основни количества, поотделно или заедно. Подходът към анализа на показателите определя техниката за измерване на температурата, която се притежава от:
Калориметрите с постоянна стойност Tc и To са от изотермичен тип и устройства, в които Tc = To се наричат адиабатични. Ако устройството работи при условия с постоянна разлика между температурите, то се нарича калориметър с постоянен поток. Механизмът на изоперибола има константа To, а Tc е термичната функция на мощността L. Крайни резултати
Има редица фактори, които могат да повлияят на крайния резултат от измерването. Едно от тях е наличието на промени, които влияят върху крайния им резултат. Това се дължи на надеждността на автоматичния набор от терморегулатори за изотермичната или адиабатна обвивка. В последния случай температурата се определя от нейната близост до променящите се условия на цялата калориметрична система. Този дизайн има лекотата на метален екран и е оборудван с нагревателно устройство, което намалява потока и стойността на топлопредаването до определено ниво, при което температурата на калориметъра ще се променя само с десетични части от градус в минута. Това може да направи възможно намаляването на топлопредаването, което се случва по време на калориметричния експеримент, до изключително ниски стойности, които могат да бъдат пренебрегнати. Разгледаните в статията устройства играят огромна роля в човешкия живот и са едно от най -значимите постижения на науката. Основната функция на калориметъра е да изследва данните за промените в температурата и да установи наличието на дефекти в процеса на пренос на топлина. Има различни начини за класифициране на тези устройства, свързани със специфични параметри, които рязко се различават един от друг. Голямо разнообразие от метали може да служи като материал за производство, например има медни калориметри, олово, стомана и други. В допълнение към чистите вещества могат да се използват и сплави. Калориметър, м. [От лат. calor - топлина и гръцки. metron - мярка] (физически). Устройство за измерване на количеството топлина. Голям речникчужди думи |
Ново
- Полоцко княжество - Руска историческа библиотека Образование и разграничение на княжеството
- Полоцко княжество - Руска историческа библиотека Образование и разграничение на княжеството
- История Кузнецки Острог история
- Понтий Пилат - пети прокуратор на Юдея
- Птолемей II Филаделф - Династия Птолемей - Древно -египетски династии - Справочник на статиите - Древноизточна война в Сирия
- Роднини на Сталин. Трагедията на семейство Сталин. Какво се случи с децата и съпругите на водача. Тайната на семейството на лидера
- Схемата на родословието на Сталин
- Автомобилен Ковровски мост
- Население на Лучегорск. Лучегорск. Историята на развитието. Култура и образование
- История на град Волгоград и неговото преименуване