Разделы сайта
Выбор редакции:
- Самостоятельная работа "показательная функция" Самостоятельная работа показательная функция мордкович
- Елизавета и Разумовский: «Мой друг нелицемерный
- Семейное дело Абрикосовых (11 фото)
- Сцепленное наследование признаков
- «Поет зима аукает» анализ Поет зима думает
- О чем российские ученые говорили с Далай-ламой XIV?
- Конфликт с классным руководителем Сына оскорбляет внук классного руководителя как быть
- Что значит вызвать огонь на себя
- Презентация на тему почему погиб титаник и столько
- Мы живём в Матрице и наш мир не реален
Реклама
| Окисление органических веществ и соединений: процесс протекания реакции и конечные продукты образования. Образование органических соединений Оборудование, реактивы, материалы |
|
Как известно, все вещества могут быть поделены на две большие категории - минеральные и органические. Можно привести большое количество примеров неорганических, или минеральных, веществ: соль, сода, калий. Но какие типы соединений попадают во вторую категорию? Органические вещества представлены в любом живом организме. БелкиВажнейшим примером органических веществ являются белки. В их состав входит азот, водород и кислород. Помимо них, иногда в некоторых белках также можно обнаружить атомы серы. Белки являются одними из важнейших органических соединений, и они наиболее часто встречаются в природе. В отличие от других соединений, белкам свойственны некоторые характерные черты. Главное их свойство - это огромная молекулярная масса. Например, молекулярный вес атома спирта составляет 46, бензола - 78, а гемоглобина - 152 000. По сравнению с молекулами других веществ, белки являются настоящими великанами, содержащими в себе тысячи атомов. Иногда биологи называют их макромолекулами. Белки являются самыми сложными из всех органических строений. Они относятся к классу полимеров. Если рассмотреть молекулу полимера под микроскопом, то можно увидеть, что она представляет собой цепь, состоящую из более простых структур. Они носят название мономеров и повторяются в полимерах множество раз. Помимо белков существует большое количество полимеров - каучук, целлюлоза, а также обычный крахмал. Также немало полимеров создано и руками человека - капрон, лавсан, полиэтилен.
Образование белкаКак же образуются белки? Они представляют собой пример органических веществ, состав которых в живых организмах определяется генетическим кодом. При их синтезе в подавляющем большинстве случаев используются различные комбинации Также новые аминокислоты могут образовываться уже когда белок начинает функционировать в клетке. При этом в нем встречаются только альфа-аминокислоты. Первичная структура описываемого вещества определяется последовательностью остатков аминокислотных соединений. И в большинстве случаев полипептидная цепь при образовании белка закручивается в спираль, витки которой располагаются тесно друг к другу. В результате образования водородных соединений она имеет достаточно прочную структуру.
ЖирыДругим примером органических веществ могут послужить жиры. Человеку известно немало видов жиров: сливочное масло, говяжий и рыбий жир, растительные масла. В больших количествах жиры образуются в семенах растений. Если очищенную семечку подсолнечника положить на лист бумаги и придавить, то на листе останется маслянистое пятно. УглеводыНе менее важными в живой природе являются углеводы. Они содержатся во всех органах растений. К классу углеводов относится сахар, крахмал, а также клетчатка. Богаты ими клубни картофеля, плоды банана. Очень легко обнаружить крахмал в картофеле. При реакции с йодом этот углевод окрашивается в синий цвет. В этом можно убедиться, если капнуть на срез картофелины немного йода. Также несложно обнаружить и сахара - они все имеют сладкий вкус. Много углеводов этого класса содержится в плодах винограда, арбузов, дыни, яблони. Они представляют собой примеры органических веществ, которые также производятся в искусственных условиях. Например, из сахарного тростника добывается сахар. А как образуются углеводы в природе? Самым простым примером является процесс фотосинтеза. Углеводы представляют собой органические вещества, в которых содержится цепь из нескольких углеродных атомов. Также в их состав входит несколько гидроксильных групп. В процессе фотосинтеза сахар неорганических веществ образуется из оксида углерода и серы.
КлетчаткаЕще одним примером органических веществ является клетчатка. Больше всего ее содержится в семенах хлопка, а также стеблях растений и их листьях. Клетчатка состоит их линейных полимеров, ее молекулярная масса составляет от 500 тысяч до 2 млн. В чистом виде она представляет собой вещество, у которого отсутствует запах, вкус и цвет. Применяется оно при изготовлении фотопленки, целлофана, взрывчатки. В организме человека клетчатка не усваивается, однако является необходимой частью рациона, поскольку стимулирует работу желудка и кишечника. Вещества органические и неорганическиеМожно привести немало примеров образования органических и Вторые всегда происходят из минералов - неживых которые образуются в глубинах земли. Они входят и в состав различных горных пород. В естественных условиях неорганические вещества образуются в процессе разрушения минералов либо органических веществ. С другой стороны, из минералов постоянно образуются вещества органические. Например, растения поглощают воду с растворенными в ней соединениями, которые в дальнейшем переходят из одной категории в другую. Живые организмы используют для питания главным образом органические вещества.
Причины разнообразияНередко школьникам или студентам нужно ответить на вопрос о том, в чем заключаются причины многообразия органических веществ. Главный фактор состоит в том, что атомы углерода соединяются между собой при помощи двух типов связей - простых и кратных. Также они могут образовывать цепи. Еще одной причиной является разнообразие различных химических элементов, которые входят в органические вещества. Кроме того, многообразие обусловлено и аллотропией - явлением существования одного и того же элемента в различных соединениях. А как образуются неорганические вещества? Природные и синтетические органические вещества и их примеры изучаются как в старших классах школы, так и в профилированных высших учебных заведениях. Образование неорганических веществ - это не такой сложный процесс, как образование белков или углеводов. Например, соду с незапамятных времен люди добывали из содовых озер. В 1791 году ученый-химик Николя Леблан предложил синтезировать ее в лабораторных условиях с использованием мела, соли, а также серной кислоты. Когда-то всем привычная сегодня сода была достаточно недешевым продуктом. Для проведения опыта было необходимо прокалить поваренную соль вместе с кислотой, а затем образовавшийся сульфат прокалить вместе с известняком и древесным углем. Другим является марганцовка, или перманганат калия. Это вещество получают в промышленных условиях. Процесс образования заключается в электролизе раствора гидроксида калия и марганцевого анода. При этом анод постепенно растворяется с образованием раствора фиолетового цвета - это и есть всем известная марганцовка. Одно из основных предположений гетеротрофной гипотезы заключается в том, что возникновению жизни предшествовало накопление органических молекул. Сегодня мы называем органическими молекулами все те молекулы, которые содержат углерод и водород. Мы называем молекулы органическими еще и потому, что первоначально считалось, что соединения такого рода могут синтезироваться только живыми организмами. Однако еще в 1828г. химики научились синтезировать мочевину из неорганических веществ. Мочевина- это органическое соединение, которое у многих животных выделяется в моче. Живые организмы считались единственным источником мочевины до тех пор, пока ее не удалось синтезировать в лаборатории. Лабораторные условия, в которых химиками были получены органические соединения, видимо, в какой-то степени имитируют условия среды на земле в ранний период ее существования. Эти условия могли, по мнению авторов гетеротрофной гипотезы, привести к образованию органических соединений из атомов кислорода, водорода, азота и углерода. Лауреат Нобелевской премии Гарольд Юри, работающий в Чикагском университете, заинтересовался вопросами эволюции химических соединений на Земле в условиях раннего периода ее существования. Он обсуждал эту проблему с одним из своих студентов- Стенли Миллером. В мае 1953 г. Миллер опубликовал статью под названием «Образование аминокислот в условиях, близких к условиям, существовавшим на Земле в ранний период», в которой указывал, что А.И. Опарин высказывал впервые идею о том, что основа жизни- органические соединения образовались в тот период, когда в атмосфере Земли были метан, аммиак, вода и водород, а не двуокись углерода, азот, кислород и вода. Недавно эта идея получила подтверждения в роботах Юри и Бернала. Для того чтобы проверить эту гипотезу, в специально созданном приборе через систему труб пропускалась смесь газов CH4, NH3, H2O и H2, и в определенный момент времени создавался электрический момент времени создавался электрический разряд. В полученной смеси определяли содержание аминокислот. В сконструированном Миллером воздухонепроницаемом приборе, наполненном метаном, водородом и аммиаком, пропускали электрический разряд. Водяной пар поступал из специального приспособления, связанного с основной частью прибора. Пар, проходя через прибор, охлаждался и конденсировался в виде дождя. Таким образом, в лаборатории были довольно точно воспроизведены условия, существовавшие в атмосфере первобытной Земли. К ним относятся тепло, дождь и кратковременные вспышки света. Через неделю Миллер проанализировал газ, который находился в экспериментальных условиях. Он обнаружил, что образовавшаяся ранее бесцветная жидкость стала красной. Химический анализ показал, что в жидкости появились некоторые соединения, которых не было в начале опыта. Атомы некоторых молекул газа рекомбинировали, образовывая новые и более сложные молекулы-органических молекул. Анализируя соединения, находящиеся в жидкости, Миллер обнаружил, что там образуются органические молекулы, известные под названием аминокислоты. Аминокислоты состоят из атомов углерода, водорода, кислорода и азота. Каждый углеродный атом способен образовать четыре химические связи с другими атомами. Опыты Миллера указывают на то, что аналогичные процессы могли происходить в атмосфере Земли в ранний период ее существования. Эти опыты явились важным подтверждением гетеротрофной гипотезы. краткое содержание других презентаций«Культура клеток и тканей растений» - Функции гормонов в каллусогенезе. Факторы, влияющие на синтез. Дифференцированные клетки. Типы культур клеток и тканей. Генетическая гетерогенность. Культуры клеток растений. Дедифференцировка. Характеристика каллусных клеток. Исторические аспекты. Образование корончатых галлов. Культура одиночных клеток. Причины асинхронности. Синтез вторичных метаболитов. Дифференцировка каллусных тканей. Физические факторы. «Листья растений» - Черешковые листья. Какой край листовой пластинки? Лист также является органом дыхания, испарения и гуттации (выделения капель воды) растения. Какой тип жилкования? Сложные листья. Охарактеризуйте лист. Листья располагаются с двух сторон черешка на некотором расстоянии друг от друга. Сидячие листья. Край листовой пластинки. Тройчатосложные. Супротивное. Мутовчатое. Жилки. Простые листья. Лист - в ботанике наружный орган растения, основной функцией которого является фотосинтез. «Классификация плодов» - Тыквина. Померанец. Классификация плодов. Органы цветковых растений. Сравните. Ягода. Яблоко. Сочные плоды. Найди лишнее. Многокостянка. Закрепление изученного материала. Костянка. Околоплодник. Репродуктивные органы. Плоды, их классификация. «Плоды и семена» - Стручок. Не позволяй душе лениться. Лабораторная работа. Тыквина. Зерновка. Знания. Костянка. Перенос. Дерево знаний. Вопросы для закрепления. Распространение разбрасыванием. Распространение водой. Признаки семян. Соплодие. Невзрачный цветок. Перенос на наружных покровах. Образование плода. Коробочка. Работа в группах. Многокостянка. Плод. Распространение с помощью ветра. Зачем семенам расселяться. «Строение побега» - Клубень. Типы почек. Формируется из почек у основания стебля. Внешнее строение побега. Органические вещества. Внутреннее строение. Развитие побега из почки. Междоузлия четко выражены. Побег. Корневой клубень. Рост стебля. Стебель. Видоизменения побега. Разнообразие побегов. Клубнелуковица. Транспорт веществ по стеблю. Корневище. Луковица. Ветвление. Луковица и клубнелуковица. Чешуи. Почка. «Задания по строению растений» - Расположение проводящих пучков. Рассмотрите рисунок и ответьте на вопросы. Горизонтальный транспорт. Подземные видоизменения побегов. Строение почек. Расположение побегов в пространстве. Растительные ткани. Ветвление побегов. Строение конуса нарастания. Внешнее строение корня. Кущение. Видоизменения корней. Рассмотрите рисунок. Дидактика для интерактивной доски по биологии. Листорасположение. ЛЕКЦИЯ 9 Образование и разложение органических веществ. (Фотосинтез, дыхание, транспирация) Рассмотрим подробнее процессы аккумуляции солнечной энергии при образовании органических веществ и рассеивании ее при разрушении этих веществ. Жизнь на Земле зависит от потока энергии, образующейся в результате термоядерных реакций, идущих в недрах Солнца. Около 1 % солнечной энергии, достигающей Земли, преобразуется клетками растений (и некоторых бактерий) в химическую энергию синтезированных углеводов. Образование органических веществ на свету называется фотосинтезом (гр. Свет, соединение) Фотосинтез – это накопление части солнечной энергии путем превращения ее потенциальную энергию химических связей органических веществ. Фотосинтез - необходимое связующее звено между живой и неживой природой. Без притока энергии от Солнца жизнь на нашей планете, подчиняясь второму закону термодинамики прекратилась бы навсегда. Сравнительно недавно (конец 18 столетия) было обнаружено, что в образующихся при фотосинтезе органических веществах соотношение углерода, водорода и кислорода таково, что на 1 атом углерода приходится как бы 1 молекула воды (откуда и название сахаров – углеводы). Считалось, что углеводы образуются из углерода и воды, а кислород выделяется из СО 2 . Позже английский медик Корнелиус ван Ниль, изучая фото синтезирующие бактерии, показал, что в результате фотосинтеза серные бактерии выделяют серу, а не кислород: Он предположил, что не СО 2 , а вода разлагается при фотосинтезе, и предложил следующее суммарное уравнение фотосинтеза: Для водорослей и зеленых растений Н 2 А - это вода (Н 2 О). Для пурпурных серных бактерий Н 2 А – сероводорюд. Для других бактерий это может быть свободный водород или другое окисляемое вещество. Эта идея в 30-х годах 20-го столетия была подтверждена экспериментально с использованием тяжелого изотопа кислорода (18 О). Для водорослей и зеленых растений суммарное уравнение фотосинтеза стали записывать следующим образом: Синтезированные растениями углеводы (глюкоза, сахароза, крахмал и др.) являются главным источником энергии для большинства гетеротрофных организмов, населяющих нашу планету. Разложение органических веществ происходит в процессе метаболизма (гр. изменение) в живых клетках. Метаболизм – это совокупность биохимических реакции и превращений энергии в живых клетках, сопровождающихся обменом веществ между организмом и средой. Сумма реакций, ведущих к распаду или деградации молекул и выделению энергии, называется катоболизмом , а приводящих к образованию новых молекул – анаболизмом. Превращения энергии в живых клетках осуществляются путем переноса электронов с одного уровня на другой или от одного атома или молекулы - к другим. Энергия углеводов выделяется в метаболических процессах при дыхании организмов. Дыхание – это процесс, в результате которого энергия, выделенная при распаде углеводов, передается на универсальную энергонесущую молекулу аденозинтрифосфорной кислоты (АТФ), где она хранится в виде высокоэнергетических фосфатных связей. Так, например, при разложении 1 моля глюкозы выделяется 686 ккал свободной энергии (1 ккал = 4,18т10 Дж). Если бы эта энергия выделялась быстро, то большая часть ее рассеялась бы в виде теплоты. Это не принесло бы пользы клетке, а привело бы к гибельному для нее увеличению температуры. Но в живых системах есть сложные механизмы, которые регулируют многочисленные химические реакции таким образом, что энергия хранится в химических связях и затем может выделяться постепенно, по мере необходимости. У млекопитающих, птиц и некоторых других позвоночных теплота, выделяемая при дыхании, сохраняется, и поэтому температура их тела выше температуры окружающей среды. У растений скорость дыхания невелика, поэтому выделяемая теплота обычно не влияет на температуру растений. Дыхание может происходить как в аэробных (в присутствии кислорода), так и в анаэробных (бескислородных) условиях. Аэробное дыхание - процесс, обратный фотосинтезу, т. е. синтезированное органическое вещество (С 6 Н 12 О 6) вновь разлагается с образованием СО 2 и Н 2 О с высвобождением потенциальной энергии Q пот аккумулированной в этом веществе: Однако в отсутствие кислорода процесс может идти не до конца. В результате такого незавершенного дыхания образуются органические вещества, еще содержащие некоторое количество энергии, которая в дальнейшем может быть использована другими организмами при других типах дыхания. Анаэробное дыхание протекает без участия газообразного кислорода. Акцептором электронов служит не кислород, а другое вещество, например уксусная кислота: запасом энергии q 1 и может использоваться в качестве топлива или самопроизвольно окисляться и воспламеняться в природе по реакции: Бескислородное дыхание служит основой жизнедеятельности многих сапротрофов (бактерий, дрожжей, плесневых грибков, простейших), но может встречаться и в тканях высших животных. Брожение - это анаэробное дыхание, при котором органическое вещество само служит акцептором электронов:
некоторое количество энергии q 2 , которая может быть использована другими организмами: Разложение может быть результатом не только биотических, но и абиотических процессов. Так, например, степные и лесные пожары возвращают большое количество СО 2 и других газов в атмосферу и минеральных веществ в почву. Они - важный и иногда даже необходимый процесс в экосистемах, где физические условия таковы, что микроорганизмы не успевают разлагать образующиеся органические остатки. Но окончательное разложение отмерших растений и животных осуществляется, в основном, гетеротрофными микроорганизмами - редуцентами, примером которых являются широко распространенные в сточных и природных водах сапрофитные бактерии. Разложение органических веществ есть результат добывания необходимых химических элементов и энергии в процессе преобразовании пищи внутри клеток их тел. При прекращении этих процессов все биогенные элементы окажутся связанными в мертвых остатках и продолжение жизни станет невозможным. Комплекс разрушителей в биосфере состоит из огромного числа видов, которые, действуя последовательно, осуществляют распад органических веществ до минеральных. Процессы образования органических веществ и их распад называют процессами продукции (лат. создание, производство) и деструкции (лат. разрушение). Продукционно-деструкционный баланс в биосфере в целом в современных условиях является положительным. Это обусловлено тем, что не все части отмерших растений и животных разрушаются с одинаковой скоростью. Жиры, сахара и белки разлагаются достаточно быстро, а древесина (клетчатка, лигнин), хитин, кости - очень медленно. Наиболее устойчивым промежуточным продуктом разложения органических веществ является гумус (лат. почва, перегной), дальнейшая минерализация которого оченьзамедлена. Медленное разложение гумуса - одна из причинзапаздывания деструкции по сравнению с продукцией. С точки зрения химии, гумусовые вещества представляют собой продуктыконденсации (лат. - скопление, уплотнение) ароматических соединений (фенолов, бензолов и др.) с продуктами распада белков и полисахаров. для их расщепления, видимо, требуютсяспециальные ферменты, которые часто отсутствуют у почвенныхи водных сапротрофов. Таким образом, разложение органических остатков - длительный, многоступенчатый и сложный процесс, который контролирует несколько важных функций экосистемы: возвращение элементов питания в круговорот и энергии - в систему; преобразование инертных веществ земной поверхности; образование безвредных комплексных соединений токсичных веществ; поддержание состава атмосферы, необходимого для жизни азробов. Для биосферы в целом важнейшее значение имеет отставание процессов разложения органических веществ от процессов синтеза их зелеными растениями. Именно это отставание обусловило накопление в недрах планеты горючих ископаемых, а в атмосфере кислорода. Установившийся в биосфере положительный баланс продукционно-деструкционных процессов обеспечивает жизнь аэробных организмов, в том числе и человека. Основные закономерности водопотребления растениями. Транспирация – это процесс испарения воды наземными частями растений. Одна из основных физиологических функций любого организма - поддержание на достаточном уровне количества воды в теле. В процессе эволюции у организмов сформировались разнообразные приспособления к добыванию и экономному расходованию воды, а также к переживанию засушливого периода. Одни животные пустыни получают воду из пищи, другие за счет окисления своевременно запасенных жиров (на пример, верблюд, способный путем биологического окисления из 100 г жира получить 107 г метаболической воды). При этом у них минимальна водопроницаемость наружных покровов тела, преимущественно ночной образ жизни и т. д. При периодической засушливости характерно впадание в состояние покоя с минимальной интенсивностью обмена веществ. Наземные растения получают воду главным образом из почвы. Малое количество осадков, быстрый дренаж, интенсивное испарение либо сочетания этих факторов ведут к иссушению, а избыток влаги - к переувлажнению и заболачиванию почв. Баланс влаги зависит от разницы между количеством выпавших осадков и количеством воды, испарившейся с поверхностей растений и почвы, а также путем транспирации. В свою очередь процессы испарения непосредственно зависят от относительной влажности атмосферного воздуха. При влажности, близкой к 100%, испарение практически прекращается, и если дополнительно понижается температура, то начинается обратный процесс - конденсация (образуется туман, выпадают роса, иней). Влажность воздуха как экологический фактор при своих крайних значениях (повышенной и пониженной влажности), усиливает воздействие (усугубляет) температуры на организм. Насыщение воздуха парами воды редко достигает максимального значения. Дефицит влажности - разность между максимально возможным и фактически существующим насыщением при данной температуре. Это один из важнейших экологических параметров, поскольку характеризует сразу две величины: температуру и влажность. Чем выше дефицит влажности, тем суше и теплее, и наоборот. Режим осадков - важнейший фактор, определяющий миграцию загрязняющих веществ в природной среде и вымывание их из атмосферы. Масса воды, содержащаяся в живых организмах, оценивается в 1,1 10 3 млрд т, т. е. меньше, чем содержат русла всех рек мира. Биоценоз биосферы, заключая в себе относительно малое количество воды, тем не менее интенсивно прогоняет ее через себя. Особенно интенсивно это происходит в океане, где вода является и средой обитания, и источником пита тельных веществ и газов. Основную массу биоценоза планеты составляют продуценты. В водных экосистемах это водоросли и фитопланктон, а в наземных - растительность. В водной среде растения непрерывно фильтруют воду через свою поверхность, а на суше они извлекают воду корнями из почвы и удаляют (транспирируют) наземной частью. Так, для синтеза одного грамма биомассы высшие растения должны испарить около 100 г воды. Наиболее мощные системы транспирации на суше - это леса, которые способны прокачать через себя всю массу воды гидросферы за 50 тыс. лет; при этом планктон океана профильтровывает всю воду океана за год, а морские организмы все вместе - всего за полгода. В биосфере работает сложный фильтр фотосинтеза, в процессе которого вода разлагается и вместе с диоксидом углерода используется при синтезе органических соединений, необходимых для построения клеток организмов. Всю массу воды гидросферы фотосинтезирующие живые организмы могут разложить примерно за 5-б млн лет, а другие организмы примерно за такой же срок восстанавливают потерянную воду из отмирающей органической массы. Таким образом, биосфера, несмотря на ничтожный объем заключенной в ней воды, оказывается самым мощным и сложным фильтром гидросферы на Земле. Каскад биологических фильтров пропускает через себя массу воды, равную массе всей гидросферы за время от полугода до миллионов лет. Поэтому можно утверждать, что гидросфера - это продукт живых организмов, среда, которую они создали сами для себя. Академик В. И. Вернадский выразил это тезисом: Организм имеет дело со средой, к которой он не только приспособлен, но которая приспособлена к нему. Развитие экосистем. Наблюдения в природе показывают, что заброшенные поля или выжженный лес постепенно завоевываются многолетними дикими травами, затем кустарниками и, в конце концов, деревьями. Развитие экосистем во времени известно в экологии под названием экологических сукцессий (лат. преемственность, последовательность). Экологическая сукцессия - это последовательная смена биоценозов, преемственно возникающих на одной и той же территории под воздействием природных или антропогенных факторов. Некоторые сообщества остаются стабильными многие годы, другие быстро изменяются. Изменения происходят во всех экосистемах естественным или искусственным путем. Естественные изменения являются закономерными и управляются самим сообществом. Если сукцессионные изменения определяются в основном внутренними взаимодействиями, то это аутогенные, т. е. самопорождающиеся сукцессии. Если изменения вызываются внешними силами на входе экосистемы (шторм, пожар, воздействие человека), то такие сукцессии называют аллогенными т. е. порожденными извне. Например, вырубка в леса быстро заселяется окружающими деревьями; луг может смениться лесом. Аналогичные явления происходят в озерах, на скальных склонах, голых песчаниках, на улицах покинутых поселков и т. п. Процессы сукцессии непрерывно идут на всей планете. Последовательные сообщества, сменяющие друг друга на данном пространстве, называются сериями или стадиями. Сукцессия, начинающаяся на участке, прежде не занятом, называется первичной. Например, поселения лишайников на камнях: под действием выделений лишайников каменистый субстрат постепенно превращается в подобие почвы, где поселяются затем кустистые лишайники, зеленые травы, кустарники и т. л. Если сообщество развивается на месте уже существовавшего, то говорят о вторичной сукцессии. Например, изменения, происходящие после раскорчевки или порубки леса, устройство пруда или водохранилища и т. п. Скорость сукцессий различна. В историческом аспекте смена фауны и флоры по геологическим периодам есть не что иное, как экологические сукцессии. Они тесно связаны с геологическими и климатическими изменениями и эволюцией видов. Такие изменения происходят очень медленно. Для первичных сукцессий требуются сотни и тысячи лет. Вторичные протекают быстрее. Сукцессия начинается с несбалансированного сообщества, у которого продукция (П) органического вещества либо больше, либо меньше скорости дыхания (Д), и сообщество стремится к состоянию, где П = Д. Сукцессия, начинающаяся при П > Д называется автотрофной , а при П <Д - гетеротрофной . Отношение П/Д является функциональным показателем зрелости экосистем. При П > Д постепенно растет биомасса сообщества (Б) и отношение биомассы к продукции Б/П, т. е- увеличиваются размеры организмов. Возрастание происходит до тех пор, пока не произойдет стабилизация системы. Состояние стабилизированной экосистемы называется климаксом (гр. лестница, зрелая ступень). Автотрофная сукцессия - широко распространенное в природе явление, которое начинается в незаселенной среде: формирование леса на брошенных землях или восстановление жизни после извержения вулканов и других природных катастроф. Она характеризуется длительным преобладанием автотрофных организмов. Гетеротрофная сукцессия характеризуется преобладанием бактерий и встречается тогда, когда среда пересыщена органическими веществами. Например, в реке, загрязняемой сточными водами с большим содержанием органических веществ, или на очистных сооружениях. При гетеротрофных сукцессиях энергетические запасы могут постепенно исчезать. Из-за отсутствия автотрофного процесса климакс может не наступить; тогда после исчерпания энергетических запасов экосистема может исчезнуть (разрушающееся дерево). В климаксных системах образуется сложная сеть взаимоотношений, поддерживающих ее стабильное состояние. Теоретически такое состояние должно бытъ постоянным во времени и существовать до тех пор, пока его не нарушат сильные внешние возмущения. Чем больше отношение П/Д отклоняется от 1, тем менее зрелой и менее устойчивой является экосистема. В климаксных сообществах это отношение приближается к 1. Тенденции изменения основных характеристик экосистем. При аутогенных сукцессиях наблюдается закономерное изменение основных признаков экологических систем (табл. 2.2).
Сукцессии связаны с функциональным сдвигом энергии в сторону увеличения затрат на дыхание, по мере того как накапливаются органическое вещество и биомасса. Общая стратегия развития экосистем состоит в возрастании эффективности использования энергии и биогенных элементов, достижении максимального разнообразия видов и усложнении структуры системы. Сукцессия- это направленное предсказуемое развитие экосистемы до установления равновесия между биотическим сообществом – биоценозом и абиотической средой – биотопом . В процессе сукцессии популяции организмов, функциональные связи между ними закономерно и обратимо сменяют друг друга. Несмотря на то, что экосистема не является «сверхорганизмом», между развитием экосистемы, популяции, организма, а также сообщества людей существует множество параллелей. Эволюция экосистем, в отличие от сукцессий, представляет собой длительный процесс исторического развития. Эволюция экосистем - это история развития жизни на Земле от возникновения биосферы до наших дней. В основе эволюции лежит естественный отбор на видовом или более низком уровне. Эволюция экосистем в какой-то степени повторяется в их сукцессионном развитии. Эволюционные процессы необратимы и нецикличны. Если сравнить состав и структуру экосистем в ранние и поздние геологические эпохи, то прослеживается тенденция увеличения видового разнообразия, степени замкнутости биогеохимических циклов равномерности распределения и сохранения ресурсов внутри системы, усложнения структуры сообществ и стремления к сбалансированному состоянию, при котором темпы эволюции замедляются. В такой системе эволюция встречает множество препятствий, т.к. сообщество плотно укомплектовано и связи между организмами и популяциями прочны. При этом шансы проникнуть в такую систему извне очень малы и ее эволюция несколько заторможена. Биомы. Физико-химические и климатические условия в разных частях биосферы различны. Климатически обусловленные крупные совокупности экосистем называют биомами, или формациями. Биом- это макросистема или совокупность экосистем, тесно связанных климатическими условиями, потоками энергии, круговоротом веществ, миграцией организмов и типом растительности. Каждый биом включает в себя ряд меньших по размеру, связанных между собой экосистем. Биомы по местообитанию подразделяют на три основные группы: наземные, морские и пресноводные. Формирование их зависит от макроклимата, а для пресноводной - от географической широты местности. Важными факторами являются: циркуляция воздуха, распределение солнечного света, сезонность климата, высота и ориентация гор, гидродинамика водных систем. Наземные биомы в основном определяются растительностью, теснейшим образом зависящей от климата и образующей основную биомассу. Четкие границы между биомами встречаются редко. Чаще они размыты и представляют широкие переходные зоны. На границе двух экосистем, например на опушке леса, одновременно встречаются представители лесных и луговых видов. Контрастность среды, а потому большое обилие экологических возможностей порождает «сгущение жизни», называемое правилом краевого эффекта или правилом экотона (от гр. дом и связь). Самый богатый по числу видов биом планеты - это вечнозеленый дождевой тропический лес. Морские биомы в меньшей степени зависят от климата, чем наземные. Они формируются в зависимости от глубины водоема и вертикального размещения организмов. Важнейшее значение имеет то, что фотосинтез возможен лишь в поверхностных горизонтах воды. Прибрежное океаническое мелководье, ограниченное с одной стороны берегом, а с другой - гребнем континентального склона (до 600 м), называется континентальным шельфом (англ. полка). Площадь шельфа составляет около 8 % от общей площади мирового океана.
В области шельфа расположена литоральная зона (лат. прибрежный). Небольшие глубины, близостъ к материкам, приливы и отливы определяют ее богатство питательными веществами, высокую продуктивность и разнообразие организмов. Здесь производится около 80 % всей биомассы океана и сконцентрирован мировой океанический промысел. От нижнего края шельфа над континентальным склоном до глубины 2 - З тыс. м простирается батиальная зона (гр. глубокий). Площадь этой зоны - чуть более 15 % от всей площади океана. По сравнению с литоралью фауна и флора батиали гораздо беднее; общая биомасса не превышает 10 % биомассы мирового океана. От подножия континентального склона до глубин 6 - 7 тыс. м находится абиссальная зона (гр. бездна) океана. Она занимает площадь более 75 % дна океана. Абиссаль характеризуется отсутствием солнечного света у дна, слабой подвижностью водных масс, ограниченностью питательных веществ, бедностью животного мира, низким видовым разнообразием, биомассой. В абиссальной области встречаются глубокие впадины – до 11 тыс. м, площадь которых около 2 % от общей площади дна океана. Пресные внутренние водоемы, как правило, неглубоки. Ведущим фактором в этих экосистемах становится скорость циркуляции воды. По этому признаку различают лотические (лат. смывающие) текучие воды (реки, ручьи) и лентические (лат, медленно, спокойно), стоячие воды (озера, пруды, лужи). Крупные биомы земного шара отличаются стабильностью.
Федеральное агентство по образованию Государственное образовательное учреждение Новгородский государственный университет им. Ярослава Мудрого Факультет естественных наук и природных ресурсов Кафедра химии и экологии образование и расход органических веществ растениями Сборник методических указаний Великий Новгород Образование и расход органических веществ растениями: Сборник методических указаний к лабораторным работам/ Составитель Кузьмина И. А. - НовГУ, Великий Новгород, 2007. – 12 с. Методические указания предназначены для студентов специальности 020801.65 - «Экология» и всех студентов, изучающих «Общую экологию». ВведениеДля образования органических веществ - основы растительной биомассы на Земле необходимы углекислый газ атмосферы и вода, а также минеральные вещества почвы. При помощи света определенной длины волн осуществляется фиксация углекислого газа у растений в процессе фотосинтеза. В результате этого выделяется в атмосферу кислород, образующийся в процессе фотолиза воды. Такова первая стадия биохимического цикла углерода. Количество энергии, запасенной на Земле благодаря фотосинтезу, огромно. Ежегодно в результате фотосинтеза зелеными растениями образуется 100 млрд. т органических веществ, в которых заключено около 450-1015 ккал солнечной энергии, преобразованной в энергию химических связей. Эти процессы сопровождаются такими грандиозными по своим масштабам явлениями, как ассимиляция растениями около 170 млрд. т углекислого газа, фотохимическое разложение около 130 млрд. т воды, из которой выделяется 115 млрд. т свободного кислорода. Кислород является основой жизни всех живых существ, которые используют его для окисления разнообразных органических соединений в процессе дыхания; выделяется при этом СО2. Это вторая стадия биохимического цикла углерода, связанная с углекислотной функцией живых организмов. При этом выделение кислорода на первой стадии примерно на порядок превышает его поглощение второй, в результате чего при функционировании зеленых растений кислород накапливается в атмосфере. Связанная автотрофами в процессе фотосинтеза энергия в дальнейшем расходуется на жизнедеятельность различных гетеротрофов, в том числе и человека, частично переходя в тепловую энергию , и запасается в ряде составляющих биосферу компонентах (растениях и почве). В биомах суши углерод при фотосинтезе наиболее сильно связывают леса (-11 млрд. т в год), затем пашня (-4 млрд. т), степи (-1,1 млрд. т), пустыни (-0,2 млрд. т). Но больше всего углерода связывает Мировой океан, который занимает около 70% поверхности Земли (127 млрд. т в год). Образовавшиеся органические вещества автотрофов поступают в пищевые цепи различных гетеротрофов и, проходя по ним, трансформируются, теряют массу и энергию (пирамиды массы, энергии), последняя расходуется на процессы жизнедеятельности всех организмов, входящих, как звенья, в состав пищевых цепей, уходит в мировое пространство в виде тепловой энергии. Органическое вещество различных живых организмов после их отмирания становится достоянием (пищей) гетеротрофных микроорганизмов. Микроорганизмы разлагают органическое вещество в процессе питания, дыхания и брожения . При разложении углеводов образуется углекислый газ, который выделяется в атмосферу из наземного разложившегося органического вещества, а также из почвы. При разложении белков образуется аммиак , который частично выделяется в атмосферу, а в основном в процессе нитрификации пополняет запасы азота в почве. Часть же органического вещества не разлагается, а образует «запасной фонд». В доисторические времена так образовались угли, газ, сланцы, а в настоящее время - торф и гумус почвы. Все вышеуказанные процессы представляет собой важнейшие этапы и фазы биохимических круговоротов (углерода, кислорода, азота, фосфора, серы и др.). Таким образом, живое вещество в процессе своего метаболизма обеспечивает стабильность существования биосферы при определенном составе воздуха, воды, почвы и без вмешательства человека этот гомеостаз экосистемы «Земля» сохранялся бы бесконечно долго. 2 Требования техники безопасностиОпыты выполняются строго в соответствии с методическим руководством. При выполнении работ следует выполнять общие правила техники безопасности для химических лабораторий. При попадании реактивов на кожу или одежду пораженный участок необходимо быстро обильно промыть водой. 3 Экспериментальная частьРабота № 1. Определение образования органического вещества в листьях растений в процессе фотосинтеза (по содержанию углерода)Фотосинтез - основной процесс аккумуляции вещества и энергии на Земле, в результате которого из СО2 и Н2О образуются органические вещества (в данной формуле - глюкоза): 6СО2 + 6Н2О + энергия света → С6Н12О6+ 602t Один из способов измерения интенсивности фотосинтеза заключается в определении образования органического вещества в растениях по содержанию углерода, который учитывается методом мокрого сжигания, разработанным для почв и модифицированный для древесных растений Ф. 3. Бородулиной. Во взятом образце листьев определяется содержание углерода, затем листья выдерживаются 2-3 ч и более на свету и снова определяется содержание углерода. Разница между вторым и первым определением, выраженная на единицу поверхности листа в единицу времени, показывает количество образовавшегося органического вещества. В процессе сжигания углерод листьев окисляется 0,4 н раствором бихромата калия в серной кислоте. Реакция протекает по следующему уравнению: 2K2Cr2О7 + 8H2SO4 + 3C = 2K2SO4 + 2Cr2(SO4)3 + 8H2O + 3СО2 Неизрасходованное количество бихромата калия устанавливают обратным титрованием 0,2 н раствором соли Мора: 6FeSO4 ∙ (NH4)2SO4 + K2Cr2O7 + 7H2SO4 = Cr2(SO4)3 + 3Fe2(SO4)3 + 6(NH4)2SO4 + K2SO4 + 7H2O В качестве индикатора применяют бесцветный раствор дифениламина, который при окислении переходит в дифенилбензидинвиолет сине-фиолетового цвета. Бихромат калия окисляет дифениламин и смесь приобретает красно-бурую окраску. При титровании солью Мора шестивалентный хром восстанавливается в трехвалентный. В результате цвет раствора переходит в синий, а к концу титрования - в сине-фиолетовый. Когда же хром будет оттитрован, последующее добавление соли Мора вызывает переход окисленной формы индикатора в восстановленную (бесцветную); появляется зеленая окраска, которую придают раствору ионы трехвалентного хрома. Четкому переходу сине-фиолетовой окраски в зеленую мешают ионы трехвалентного железа, появляющиеся в процессе реакции. Чтобы сделать более ясным конец реакции титрования ее проводят в присутствии ортофосфорной кислоты, которая связывает ионы Fe3+ в бесцветный комплексный ион 3-и предохраняет дифениламин от окисления. Оборудование, реактивы, материалы: 1) конические колбы на 250 мл; 2) термостойкие конические колбы на 100 мл; 3) маленькие стеклянные воронки, используемые как обратные холодильники; 4) бюретки; 5) 0,4 н раствор бихромата калия (в разбавленной серной кислоте (1:1)); 6) 0,2 н раствор соли Мора; 7) дифениламин; 8) 85%-ная ортофосфорная кислота; 9) пробочное сверло или другое приспособление для выбивания дисков диаметром 1 см; 10) мерный цилиндр; 11) вегетирующие растения с симметричной широкой и тонкой листовой пластинкой (герань, фуксия, листья древесных растений). Ход работы Лист вегетирующего растения делят на две половинки вдоль главной жилки и на одной из них вырезают пробочным сверлом 3 диска диаметром 1 см, помещают на дно конической термостойкой колбочки объемом 100 мл, куда наливают 10 мл 0,4 н раствора К2Сr2О7. Колбу закрывают маленькой воронкой носиком вниз и ставят на электроплитку с закрытой спиралью в вытяжной шкаф. Когда раствор закипит, добиваются слабого кипения в течение 5 мин, иногда слегка взбалтывают колбу круговым движением, чтобы диски были хорошо покрыты жидкостью. По верху колбы (не закрывая горлышко) укрепляют поясок из нескольких слоев плотной бумаги, который предотвратит ожог рук при помешивании содержимого колбы и при ее перестановке. Затем колбу снимают с нагрева, ставят на керамическую плитку и охлаждают. Жидкость должна быть буроватого цвета. Если окраска ее зеленоватая, то это указывает на недостаточное количество бихромата калия, взятого для окисления органического вещества. В этом случае определение нужно повторить с большим количеством реактива или меньшим количеством высечек. К охлажденному раствору небольшими порциями в несколько этапов приливают 150 мл дистиллированной воды, затем эту жидкость постепенно переливают в колбу на 250 мл, куда добавляют 3 мл 85%-ной ортофосфорной кислоты и 10 капель дифениламина. Взбалтывают содержимое и оттитровывают 0,2 н раствором соли Мора. Одновременно проводят контрольное определение (без растительного материала), тщательно соблюдая все указанные выше операции. Соль Мора сравнительно быстро теряет титр, поэтому раствор необходимо периодически проверять перед началом определения. Количество углерода органического вещества, содержащегося в 1 дм2 листовой поверхности, рассчитывают по формуле:
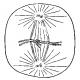
а - количество соли Мора в мл, израсходованное на титрование контрольного раствора; b - количество соли Мора в мл, пошедшее на титрование опытного раствора; k - поправка к титру соли Мора; 0,6 - миллиграммы углерода, соответствующие 1 мл точно 0,2 н раствора соли Мора; S - площадь высечек, см2. Схема записи результатов Пример расчета количества углерода: 1. В начале опыта: а = 19 мл, b = 9 мл, k = 1, S = πr2∙3 = (3,14 ∙ 12) ∙ 3 = 9,4 см2 Водород" href="/text/category/vodorod/" rel="bookmark">водород улетучиваются в виде углекислого газа, воды и окислов азота. Оставшийся нелетучий остаток (зола) содержит элементы, называемые зольными. Разница между массой всего сухого образца и зольным остатком составляет массу органического вещества. 1) аналитические или точные технохимические весы; 2) муфельная печь; 3) тигельные щипцы; 4) электроплитка с закрытой спиралью; 5) фарфоровые тигли или испарительные чашки; 6) препаровальные иглы; 7) эксикатор; 8) спирт; 9) дистиллированная вода; 10) хлористый кальций; 11) высушенные до абсолютно сухой массы стружка древесины, измельченная кора, листья, гумусированная почва. Ход работы Сухие и измельченные образцы древесины, коры, листьев, а также почвы (3-6 г и более), отобранные методом средней пробы, взвешиваются до 0,01 г на кальке. Их помещают в прокаленные и взвешенные фарфоровые тигли или испарительные чашки (диаметром 5-7 см), подписанные 1 %-ным раствором хлорного железа, которое при нагревании буреет и при прокаливании не исчезает. Тигли с органическим веществом ставят на разогретую электроплитку в вытяжной шкаф и прогревают до обугливания и исчезновения черного дыма. При этом при наличии большего количества растительного материала возможно его дополнение из предварительно взвешенного образца. Затем тигли ставят в муфельную печь при температуре 400-450° С и сжигают еще 20-25 мин до того состояния, когда зола станет серо-белой. При более высокой температуре прокаливания могут быть существенные потери серы, фосфора, калия и натрия. Может также наблюдаться сплавление с кремниевой кислотой, что мешает полному озолению. В этом случае прокаливание прекращают, охлаждают тигель и добавляют в него несколько капель горячей дистиллированной воды; подсушивают на плитке и продолжают прокаливание. Возможны следующие варианты цвета золы: красно-бурый (при большом содержании в образце окислов железа), зеленоватый (в присутствии марганца), серо-белый. При отсутствии муфельной печи сжигание можно проводить в учебных целях на электроплитке под тягой. Для создания более высоких температур надо оградить плитку вплотную железным листом в виде бортика высотой 5-7 см от полотна плитки, а также прикрыть сверху куском асбеста. Сжигание проводится 30-40 мин. При сжигании необходимо периодическое помешивание материала препаровальной иглой. Сжигание также проводится до белой золы. В случае медленного сжигания в охлажденные тигли наливается небольшое количество спирта и поджигается. В золе не должно быть заметно черных частичек угля. В противном случае пробы обрабатывают 1 мл дистиллированной воды, помешивают и повторяют прокаливание. После того как сжигание будет окончено, тигли охлаждают в эксикаторе с крышкой и взвешивают. Ведомость" href="/text/category/vedomostmz/" rel="bookmark">ведомость , вычерченную на доске. Схема записи результатовРабота № 3. Определение расхода органического вещества растениями при дыханииЛюбое сообщество живых организмов на Земле характеризуется его продуктивностью и устойчивостью. Продуктивность определяется, в частности, как разность между накоплением и расходованием органического вещества при таких кардинальных процессах, как фотосинтез и дыхание. В первом процессе органическое вещество синтезируется из углекислого газа и воды с выделением кислорода, во втором - разлагается за счет окислительных процессов, проходящих в митохондриях клеток с поглощением кислорода. Разные растения сильно различаются по соотношению этих процессов. Так, у С4 растений (кукуруза, сорго, сахарный тростник, мангровые деревья) наблюдается высокая интенсивность фотосинтеза при небольшом световом дыхании, что обеспечивает их высокую продуктивность по сравнению с С3 растениями (пшеница, рис). С3 - растения. Это большинство растений Земли, осуществляющие С3 - путь фиксации углекислого газа в процессе фотосинтеза, в результате чего образуются трехуглеродные соединения (глюкоза и др.). Это преимущественно растения умеренных широт оптимум температуры которых +20…+25°С, а максимум +35…+45°С. С4 - растения. Это те, у которых продуктами фиксации СО2 являются четырехуглеродистые органические кислоты и аминокислоты. Сюда относятся преимущественно тропические растения (кукуруза, сорго, сахарный тросник, мангровые деревья). С4 - путь фиксации СО2 сейчас обнаружен у 943 видов из 18 семейств и 196 родов, в том числе и у ряда злаковых растений умеренных широт. Эти растения отличаются очень высокой интенсивностью фотосинтеза, выносят высокие температуры (оптимум их +35…+45°С, максимум +45…+60°С). Они очень приспособлены к жарким условиям, эффективно используют воду, хорошо выносят стрессы - засуху, засоление, отличаются повышенной интенсивностью всех физиологических процессов, что предопределяет их очень высокую биологическую и хозяйственную продуктивность. Аэробное дыхание (с участием кислорода) - процесс обратный фотосинтезу. В этом процессе синтезированные в клетках органические вещества (сахароза, органические и жирные кислоты) разлагаются с высвобождением энергии: С6Н12О6 + 6О2 → 6СО2 + 6Н2О + энергия Все растения и животные получают энергию для поддержания своей жизнедеятельности с помощью дыхания. Метод определения интенсивности дыхания у растений основан на учете количества выделяемого растениями углекислого газа, который поглощается баритом: Ва(ОН)2 + СО2 = ВаСО3 + Н2О Избыток барита, не прореагировавшего с СО2, оттитровывают соляной кислотой: Ва(ОН)2 + 2HCl = ВаС12 + Н2О Оборудование, реактивы, материалы1) широкогорлые конические колбы емкостью 250 мл; 2) резиновые пробки с просверленными отверстиями, в которые вставляется стеклянная трубка; в трубку протягивается тонкая проволока длиной 12-15 см; 3) весы технохимические; 4) разновесы; 5) черная светонепроницаемая бумага; 6) бюретки с раствором Ва(ОН)2 и пробкой сверху, в которую вставлена трубка с натронной известью; 7) 0,1 н раствор Ва(ОН)2; 8) 0,1 н раствор HCI; 9) 1%-ный раствор фенолфталеина в капельнице; 10) зеленые листья, только что сорванные в природной обстановке или листья комнатных растений . Ход работы 5-8 г зеленых, только что сорванных листьев растений взвешивают с черешками на технохимических весах, черешки скрепляют одним концом проволоки, которую протягивают через отверстие пробки (рис. 1).
Рис. 1. Смонтированная колба для определения интенсивности дыхания: 1 - проволока, 2 - стеклянная трубка, 3 - резиновая пробка, 4 - пучок листьев, 5 - барит. Предварительно рекомендуется провести пробную установку, опуская материал в колбу и закрывая колбу пробкой. Обратить внимание, чтобы пробка плотно закрывала колбу, пучок листьев располагался в верхней части колбы и расстояние между баритом и пучком было достаточно велико. Все отверстия между колбой, пробкой и трубочкой рекомендуется заделать пластилином, а в месте верхнего выхода проволоки из трубки изолировать систему кусочком фольги. В опытные колбы наливается из бюретки по 10 мл 0,1 н раствора Ва(ОН)2, помещается материал и изолируется вышеуказанным способом. Контроль (без растений) ставится в 2-3-кратной повторности. Все колбы закрывают черной светонепроницаемой бумагой для исключения фотосинтеза и идентичности всех колб, отмечается время начала опыта, который длится 1 ч. В течение опыта следует периодически осторожно покачивать колбы, чтобы разрушить пленку ВаСО3, образующуюся на поверхности барита и препятствующую полноте поглощения СО2. Через один час приоткрыть пробку и извлечь из колб материал путем быстрого выдергивания проволоки с листьями. Немедленно закрыть пробку, изолировав верх трубочки фольгой. Перед титрованием добавить в каждую колбу по 2-3 капли фенолфталеина: раствор окрашивается в малиновый цвет. Оттитровать свободный барит 0,1 н HCl. При этом первыми оттитровывают контрольные колбы. Вывести среднее, а затем оттитровать опытные колбы. Титровать растворы следует осторожно до обесцвечивания. Результаты записать в таблицу (на доске и в тетради). Конечный продукт" href="/text/category/konechnij_produkt/" rel="bookmark">конечных продуктов Другой формой распада органического вещества до простейших соединений являются микробиологические процессы в почвах и водах, в результате чего образуется гумус почвы и различные донные отложения полуразложившейся органики (сапропель и др.). Основные из этих процессов - биологическое разложение сапрофитами органических веществ, содержащих азот и углерод, что является составной частью круговоротов этих элементов в природных циклах. Бактерии-аммонификаторы минерализуют белки растительных и животных остатков, а также других микроорганизмов (в том числе и азотфиксаторов), мочевину, хитин, нуклеиновые кислоты, в результате чего образуется аммиак (NH3). Разлагаются и содержащие серу белки растений и животных, в результате чего образуется сероводород (H2S). Продуктом жизнедеятельности микроорганизмов являются и индольные соединения, которые выполняют роль стимуляторов роста. Наиболее известна β-индолилуксусная кислота или гетероауксин. Индольные вещества образуются из аминокислоты триптофана. Процесс разложения органических веществ до простых соединений - ферментативный. Конечным этапом аммонификации являются аммонийные соли, доступные для растений. Оборудование, реактивы, материалы 1) весы технохимические; 2) термостат; 3) пробирки; 4) ватные пробки; 5) химические стаканы; 6) чашки Петри; 7) NaHCO3;8) 5%-ная PbNO3 или Рb(СН3СОО)2; 9) реактив Сальковского; 10) реактив Эрлиха; 11) нингидриновый реактив; 12) реактив Несслера; 13) гумусная почва; 14) свежие листья люпина или засушенные листья других бобовых; 15) рыбная, мясная мука или кусочки мяса, рыбы. Ход работыА. Аммонификация животных белков а) Поместить в пробирку 0,5-1 г свежей рыбы или маленький кусочек мяса. Добавить отстоянной воды до половины объема пробирки и 25-50 мг NaHCO 3 (на кончике скальпеля) для нейтрализации среды, что благоприятствует деятельности аммонификаторов (благоприятна для них нейтральная или слабощелочная среда при рН=7 и выше). Прибавить небольшой комочек гумусной почвы для введения в среду аммо-нификаторов, смешать содержимое пробирки, заткнуть пробирку ватной пробкой, предварительно укрепив между пробкой и пробиркой кусочек свинцовой бумажки (рис. 2) так, чтобы он не касался раствора. Каждую пробирку вверху обернуть фольгой, чтобы исключить выход газа из пробирки. Поставить все в термостат при 25-30°С на 7-14 дней.
Рис. 2. Смонтированная пробирка для определения аммонификации белков: 1 - пробирка; 2 - ватная пробка; 3 - свинцовая бумажка; 4 - среда. Этот опыт имитирует разложение органических остатков в водной среде стоячего водоема (например, пруд), куда могут попадать частички почвы с прилегающих полей путем смыва. б) Насыпать гумусную почву в стаканчик, полить отстоянной водой, закопать в почву небольшой кусочек мяса, укрепить свинцовую бумажку между почвой и краем стаканчика, закрыть систему чашкой Петри (бортиком вниз), поставить в термостат при 25-30°С на одну - две недели. Этот опыт имитирует разложение органических остатков (червей, различных почвенных животных) в почве. Б. Аммонификация растительных остатков Проследить разложение в почве зеленого удобрения, для чего наполнить химический стакан на 100 мл гумусовой почвой и закопать в нее несколько кусочков зеленых стеблей и листьев многолетнего люпина, гороха, фасоли, посаженного с осени в горшок. Можно использовать распаренные в воде сухие части бобовых растений летнего сбора. Закрыть стаканы крышкой от чашки Петри, поместить в термостат при температуре 25-30°С на одну - две недели, поддерживая нормальную влажность почвы в течение опыта (60% от полной влагоемкости), не переувлажняя ее. Продолжение работы № 4 (проводится через 7-14 дней) а) Отфильтровать часть культурального раствора из пробирок, в которых происходило разложение животных белков. Обратить внимание на образование плохо пахнущих продуктов (сероводород - запах тухлых яиц, индольные соединения и др.). Обнаружить образование аммиака добавлением к 1 мл культурального раствора 2-3 капель реактива Несслера. Для этого удобно использовать часовое стекло, помещенное на лист белой бумаги, или фарфоровую чашку. Пожелтение раствора свидетельствует о наличии аммиака, образовавшегося при разрушении белков. Обнаружить наличие сероводорода по почернению свинцовой бумажки над раствором или при опускании ее в раствор. Накапать культуральный раствор на фильтровальную или хро-матографическую бумагу микропипеткой с оттянутым носиком (10-20 капель в одну точку), подсушить над вентилятором , капнуть реактива Сальковского, Эрлиха или нингидринового реактива. Подогреть над плиткой. Индольные соединения с реактивом Сальковского дают синее, красное, малиновое окрашивания в зависимости от состава индольного продукта (ауксин индолилуксусная кислота дает красное окрашивание). Реактив Эрлиха дает с индольными производными пурпурное окрашивание. Нингидриновый реактив - это реакция на аминокислоту триптофан (предшественник индольных ауксинов). При подогреве - синее окрашивание. б) Извлечь из почвы кусочек мяса или рыбы вместе с почвой, прилегающей к кусочку, поместить в стаканчик, налить немного воды, помять стеклянной палочкой, взболтать, отфильтровать. Определить в фильтрате аммиак, сероводород, индольные вещества вышеуказанными методами. Сходные процессы происходят в почве при перегнивании отмерших животных. в) Извлечь из почвы полуразложившиеся стебли люпиновой зеленой массы, очистить от почвы и растереть с небольшим количеством воды. Отфильтровать 1-2 мл раствора и сделать пробу на аммонийный азот, освобождающийся при минерализации растительных белков (с реактивом Несслера). Сходные процессы происходят в почве при запахивании зеленого удобрения или органических остатков в виде навоза, торфа, сапропеля и др. Определить наличие сероводорода, индольных веществ, триптофана. г) Поместить на предметное стекло каплю культуральной жидкости из пробирки, где происходило разложение животного белка, и изучить ее под микроскопом при увеличении 600. Обнаруживаются многочисленные микроорганизмы, вызывающие разложение органических веществ. Часто они энергично движутся и червеобразно изгибаются. Введение. 3 2 Требования техники безопасности. 4 3 Экспериментальная часть. 4 Работа № 1. Определение образования органического вещества в листьях растений в процессе фотосинтеза (по содержанию углерода) 4 Работа № 2. Определение накопления органического вещества в биомассе растений и в почве. 8 Работа № 3. Определение расхода органического вещества растениями при дыхании 11 Работа № 4. Разложение органических веществ воды и почвы с определением некоторых конечных продуктов. 14 |
||||||||||
| Читайте: |
|---|
Популярное:
Новое
- Елизавета и Разумовский: «Мой друг нелицемерный
- Семейное дело Абрикосовых (11 фото)
- Сцепленное наследование признаков
- «Поет зима аукает» анализ Поет зима думает
- О чем российские ученые говорили с Далай-ламой XIV?
- Конфликт с классным руководителем Сына оскорбляет внук классного руководителя как быть
- Что значит вызвать огонь на себя
- Презентация на тему почему погиб титаник и столько
- Мы живём в Матрице и наш мир не реален
- Русские земли и княжества в XII - первой половине XIII в