Sitenin bölümleri
Editörün Seçimi:
- Uluslararası çevre yasal koruma içeriğini sıkmak
- Federal bölgesinin Kamenka şehrine ait olduğu Kamenka (Penza Bölgesi)
- XII - XIII yüzyıllarında Rus ilkeleri ve arazi
- Charles de Gaulle: Biyografi ve Charles De Gaulle'in hayatından ilginç gerçekler
- Su ısıtıcısında su nerede kayboluyor?
- Oksidasyon derecesi (oksidatif numara, oksidasyon durumu) H202, oksidasyon derecesidir.
- Biyolojik Araştırma Tarihi
- Hidrojen İletişimi Tüm Örnekleri
- Barbar Ansiklopedisi: Commod, İmparator Lucius Ely Aureli Commoda Mark Azeri Oğul
- Yaratılış ve Kalkınma Tarihi
Reklâm
| Moleküller moleküller moleküler spektrumlarında bağlar. Moleküllerin yapısı ve spektrumları. Kimyasal bağlar ve moleküller |
|
Spektrumbazı enerji durumlarından başkalarına atomların ve moleküllerin geçişlerinde emilen, ayırt edici, dağınık veya yansıtılan elektromanyetik radyasyon enerjisi qualta dizisi dizisi denir. Işığın bir maddeyle etkileşiminin niteliğine bağlı olarak, spektrumlar absorpsiyon spektrumuna (absorpsiyon) ayrılabilir; emisyon (emisyon); saçılma ve yansıma. Optik Spektroskopisi, yani 10 -3 ÷ 10 -8 Dalga Boyu Bölgesinde Spektroskopisi m.atomik ve moleküler ayrılmıştır. Atomik spektrumkonumu, elektron geçiş enerjisi tarafından bazı seviyelerden başkalarına göre belirlenen bir çizgi dizisidir. Atom enerjisiÇeviri hareketinin ve enerjilerinin kinetik enerjisinin toplamı olarak sunulabilir: nerede - frekans - dalga boyu dalga numarasıdır, ışık hızı, sabit bir tahtadir. Atomdaki elektron enerjisi, ana kuantum sayısının karesi ile ters orantılı olduğundan, denklem atomik spektrumda kaydedilebilir:
Buraya Atomik spektrumun tüm satırları, kısa dalga bölgesinde, katı spektrumun giderildikten sonra atom iyonizasyon enerjisi tarafından belirlenen sınıra dönüştürür. Molekül enerjisiİlk yaklaşımda, ilerici, dönme, salınım ve enerjilerin toplamı olarak düşünebilirsiniz:
Çoğu molekül için, böyle bir durum yapılır. Örneğin, H2 291K'da, tam enerjinin bireysel bileşenleri, büyüklük sırasına göre farklılık gösterir ve daha fazlası: 309,5 kJ / Mole
2,5 kJ / Mole
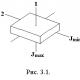
Spektrumun çeşitli alanlarında Quanta enerjisinin değerleri Tablo 4.2'de karşılaştırılır. Tablo 4.2 - Moleküllerin optik spektrumunun çeşitli alanlarının emilen kuantasının enerjisi "Çekirdek salınımları" ve "moleküllerin rotasyonu" kavramları şartlıdır. Aslında, bu tür hareket türleri, yalnızca çekirdeğin dağılımı, elektronların dağılımı olarak aynı olasılık karakterini giyen uzayda dağılımı ile ilgili fikirlerin iletilmesidir. Bir diyatomik molekül durumunda bir şematik enerji seviyesi sistemi, Şekil 4.1'de sunulmuştur. Enerji seviyeleri arasındaki geçişler, uzak IR ve mikrodalga bölgelerinde dönme spektrumlarının ortaya çıkmasına neden olur. Aynı elektron seviyesindeki osilatör seviyeleri arasındaki geçişler, yakın IR bölgesinde titreşim ve dönme spektrumları verir, çünkü osilatör kuantum numarasındaki değişiklik kaçınılmaz olarak değişikliği ve dönme kuantum numarasını gerektirir. Son olarak, elektronik seviyeler arasındaki geçişler, elektron salınımlı-dönme spektrumlarının görünür ve UV bölgelerindeki görünüme neden olur. Genel durumda, geçiş sayısı çok büyük olabilir, ancak aslında hepsi spektrumda görünmüyor. Geçiş sayısı sınırlıdır seçim kuralları . Moleküler spektrumlar zengin bilgiler verir. Kullanılabilirler: Yüksek kaliteli analizde maddeleri tanımlamak için, çünkü Her maddenin kendine özgü bir spektrumuna sahiptir; Kantitatif analiz için; Yapısal ve grup analizi için, örneğin\u003e C \u003d O, _ NH2, _H, vb. Gibi bazı gruplar için, karakteristik bantlar spektrumda verilmiştir; Moleküllerin ve moleküler özelliklerin enerji durumlarını belirlemek (etkileşim mesafesi, atalet anı, kendi salınımların kendi frekansları, ayrışma enerjisi); Kapsamlı çalışma moleküler spektrumlar Moleküllerin mekansal yapısı hakkında sonuç çıkarmanıza izin verir; Çok hızlı reaksiyonları incelemek de dahil olmak üzere kinetik çalışmalarda.
Salınım seviyelerinin enerjisi; Rotasyonel kuralların enerjileri Şekil 4.1 - Diatomik molekülün enerji seviyelerinin şematik konumu Buger-Lambert-Bera Hukuku Moleküler spektroskopisi kullanılarak nicel moleküler analizin temeli buger-Lambert-Bera Hukuku Düşen ışığın yoğunluğunu bağlayın ve emici tabakanın konsantrasyonu ve kalınlığı ile geçti (Şekil 4.2): veya orantılılık oranı ile: Entegrasyonun sonucu:
Siparişe göre düşen ışığın yoğunluğunda azalma ile
Eğer \u003d 1 mol / l, sonra, yani Emilim katsayısı, 1 konsantrasyonda, olay ışığının yoğunluğunun bir sıraya göre azaldığı ters katman kalınlığına eşittir. Emme katsayıları ve dalga boyuna bağlıdır. Bu bağımlılığın görünümü, maddeyi tanımlamak için yüksek kaliteli analizlerde kullanılan moleküllerin bir tür "parmak izi" türüdür. Bu bağımlılık da bir madde için bireydir ve molekülde bulunan karakteristik grupları ve bağlantıları yansıtır. Optik yoğunluk D. olarak ifade edildi% 4.2.3 Sert rotator yaklaşımındaki boyutsal molekülün dönme enerjisi. Moleküllerin dönme spektrumları ve bunların moleküler özelliklerini belirlemek için kullanımı Dönme spektrumlarının ortaya çıkması, molekülün dönme enerjisinin kuantum olduğu gerçeğinden kaynaklanmaktadır.
Noktadan beri Ö. Molekülün ağırlık merkezidir, o zaman: Yukarıdaki kütlenin sembolünün tanıtılması:
denklem yol açar
Böylece, boyutsal molekül (Şekil 4.7) fakat), eksen etrafında dönen veya yerçekimi merkezinden geçerek, çevresindeki bir yarıçap olan bir kütleye sahip bir partikül olarak kolayca görülebilir. Ö. (Şekil 4.7. b.). Eksen çevresindeki molekülün dönmesi, atomların radyosu interstisyel mesafeden önemli ölçüde az olduğu için neredeyse sıfıra eşit atalet momentini verir. Eksenlerin veya molekülün karşılıklı dik çizgilerinin dönmesi, ataletin anlarının büyüklüğüne eşittir: nerede - sadece tamsayı değerleri alan rotasyonel kuantum numarası 0, 1, 2 .... Uyarınca rotasyonel spektrum için seçim kuralı enerji kuantumunu emerken dönme kuantum numarasındaki çift molekül değişimi, yalnızca bir tarafından mümkündür. denklemleri (4.37) formda dönüştürür:
rotasyonel spektrumdaki çizginin dalga sayısı, geçiş sırasında kuantumun emilimine karşılık gelir j. Seviye başına enerji seviyesi j.+1, denklem ile hesaplanabilir: Böylece, sert rotator modelinin yaklaşımındaki dönme spektrumu, birbirinden aynı mesafede bulunan bir satır sistemidir (Şekil 4.5B). Modelleme rotatorunda tahmin edilen diatomik moleküllerin dönme spektrumlarının örnekleri, Şekil 4.6'da sunulmuştur.

Şekil 4.6 - Dönme Spektrumları Hf. (fakat) BEN. Coşku(b.) Halojen üreme molekülleri için, bu spektrum, mikrodalgaya ağır moleküller için, spektrumun uzak IR bölgesine kaydırılır. Diatomik molekülün dönme spektrumunun devam eden kalıplarına dayanarak, pratikte, önce spektrumdaki bitişik çizgiler arasındaki mesafeyi, ayrıca bulundukları ve denklemlerle olan mesafeyi belirler:
nerede - sabit santrifüj bozulma
dönme sabiti yaklaşık oranı ile ilgilidir Genel olarak multiyotomik moleküller için, üç farklı anı atalet varlığına sahip olmak mümkündür. nerede İzotopik kayma büyüklüğünü hesaplamak için, izotop sübstitüe edilmiş molekülün elde edilen kütlesini, izotopun atomik kütlesinin, atalet momentinin, sabit ve çizginin pozisyonundaki değişimi dikkate alarak sırayla hesaplamak gerekir. Molekülün, denklemlerle (4.34), (4.35), (4.39) ve (4.43), sırasıyla, izotop-ikameli ve kullanılmayan moleküllerde aynı geçişi karşılayan dalga sayılarının oranını değerlendirin ve ayrıca İzotopik kayma yönünü ve değerini denklem (4.50) ile tanımlayın. Interreterity mesafesi kalıcı olarak kabul edilirse toplam parçacık sayısı nerededir - parçacıkların sayısı bEN.- Sıcaklıkta hacim enerji seviyesi T., k.- Kalıcı Boltzmann, - İstatistiksel sili. dejenerasyon derecesi bEN.Enerji seviyesi, verilen seviyeye partikül bulma olasılığını karakterize eder. Dönme durumu için, seviye nüfusu tipik olarak, partikül sayısının oranı ile karakterize edilir. j.- Sıfır seviyesindeki partikül sayısına enerji seviyesi:
nerede Extremum fonksiyonu, maksimum göreceli nüfuslu seviyeye karşılık gelir, kuantum sayısının değeri, ekstremyumdaki türev fonksiyonun belirlenmesinden sonra elde edilen denklem ile hesaplanabilendir:
Şekil 4.7 - Rotasyonel enerji seviyelerinin göreceli nüfusu moleküller Coşku298 ve 1000 arasındaki sıcaklıklarda Misal.Dönme spektrumunda, bitişik çizgiler arasındaki mesafe belirlenir Karar Sert rotator modelinin denklemine uygun olarak yaklaşmasında (4.45), dönme sabitini belirliyoruz:
Molekülün atalet momenti, Denklem (4.46) ile dönme sabitinin değerinden hesaplanır:
Denge interstisyel mesafesini belirlemek için, hidrojen çekirdeğinin kütlelerinin göz önüne alındığında denklemi (4.47) kullanın. Misal.Spektrumun uzak IR bölgesinde, 1 H 35C CL, çizgiler bulundu, dalga sayıları bulunur: Atalet anının ortalama değerlerini ve molekülün interstisyel mesafesini belirleyin. Spektrumdaki gözlenen çizgileri dönme geçişlerine götürün. Karar Sert rotator modeline göre, dönme spektrumunun bitişik çizgilerinin dalga sayısındaki fark sabittir ve 2'ye eşittir. Dönme sabitini, spektrumdaki bitişik çizgiler arasındaki ortalama mesafelerle tanımlarız:
Molekülün atalet momentini buluruz (denklem (4.46)): Hidrojen çekirdeğinin kütlelerinin dikkatini çekerek denge interstisyel mesafesini (denklem (4.47)) hesaplıyoruz. Denklem (4.43) ile, 1H35 CL dönme spektrumundaki çizgilerin konumunu tahmin ediyoruz: Dalga sayısının deneysellerinin deneysel değerlerini deneysel olarak yeniden şekillendirin. Rotasyonel spektrumda gözlenen çizgilerin 1 saat 35 CR, geçişlere karşılık geldiği ortaya çıktı:
Misal.Absorpsiyon çizgisinin izotopik kaymasına, geçişe karşılık gelen değeri ve yönünü belirleyin. Karar Geçişe karşılık gelen çizginin izotopik kayması büyüklüğünü belirlemek sonra, atalet momentini, rotasyonel sabit ve hattın pozisyonunu hesaplayın Bir inakisotop kayması, moleküllerde aynı geçişi (sabit olarak düşündüğümüz mesafe mesafesi) karşılayan dalga sayısının (sabit) aynı şekilde karşılayan satırların oranı ve ardından denklem (4.51) kullanılarak hattın konumunu tahmin etmesi tahmin edilmektedir. Moleküller için 1 H 35CL ve 1H37C1, belirtilen geçişin dalga sayısının oranı:
İzotop ikame edilmiş molekülün çizgisinin dalga sayısını belirlemek için önceki örnekte bulunan dalga sayısının değerini değiştiriyoruz. j. → j.+1 (3→4): Biz sonucuna varıyoruz: düşük frekansta veya uzun dalga bölgesinde izotopik kayma 85.384-83.049 \u003d 2.335 cm -1. Misal.1H 35 CL molekülün dönme spektrumunun en yoğun spektral hattının dalga sayısını ve dalga boyunu hesaplayın. Hattı uygun rotasyonel geçişle ilişkilendirin. Karar Molekülün dönme spektrumundaki en yoğun çizgi, dönme enerji seviyesinin maksimum nispi popülasyonu ile ilişkilidir. İkame, 1 saat 35 CL için dönme sabitinin değerinin önceki örneğinde bulundu (
Bu seviyeden gelen dönme geçişinin dalga sayısı denklem ile hesaplanır (4.43): Geçişin dalga boyu, denkleme göre dönüştürülmüş olarak bulunur (4.11): 4.2.4 MultivariArt Görev Numarası 11 "Diatomik Moleküllerin Rotasyonel Spektrumları" 1. Diatomik molekülün dönme hareketinin enerjisini sert bir rotator olarak hesaplamak için kuantum-mekanik bir denklem yazın. 2. Diatomik molekülün dönüşündeki değişikliği, yakındaki, daha yüksek kuantum seviyesine geçirirken sert bir rotator olarak döndüründeki değişikliği hesaplamak için denklemi yazdırın. 3. DAATOMİK molekülün emme spektrumundaki Dalga sayısının Dalga sayısının Denklemi Denklemini, dönme kuantum sayısından çıktı. 4. Diatomik molekülün dönme emme spektrumundaki bitişik çizgilerin dalga sayısındaki farkı hesaplamak için denklemi çıktı. 5. Diatomik molekülün dönme sabitini (cm --1 ve m-1 cinsinden) hesaplayın. A. Molekülün dönme emme spektrumunun uzun dalga kızılötesi bölgesindeki iki bitişik çizginin dalga sayısına göre (bkz. Tablo 4.3). 6. Molekülün dönme enerjisini belirleyin A. İlk beş kuantum dönme seviyesinde (J). 7. Diatomik molekülün dönme hareketinin şematik enerji seviyelerini sert bir rotator olarak çizin. 8. Sert bir rotator noktalı çizgisi olmayan molekülün dönme kuantum seviyelerini uygulayın. 9. Denklem interstisyel mesafesini, dönme emme spektrumundaki bitişik çizgilerin dalga sayısındaki farkın temelinde hesaplamak için denklemi çıktı. 10. Diatomik molekülün atalet momentini (kg. M2) belirleyin. A.. 11. Molekülün elde edilen kütlesini (kg) hesaplayın A.. 12. Moleküllerin denge interstisyel mesafesini () hesaplayın A.. Elde edilen değeri referans verileriyle eşleştirin. 13. Gözlenen çizgileri molekülün dönme spektrumunda alın A. dönme geçişlerine. 14. Seviyeden dönme geçişine karşılık gelen spektral hattın dalga sayısını hesaplayın. j. Molekül için A.(Bkz. Tablo 4.3). 15. Bir izotop ikame edilmiş molekülün üretilen kütlesini (kg) hesaplayın B.. 16. Dönüş seviyesi iletim ile ilişkili spektral hattın dalga sayısını hesaplayın j. Molekül için B.(Bkz. Tablo 4.3). Moleküller interstisyel mesafeler A. ve B. Eşit düşünün. 17. Moleküllerin dönme spektrumundaki izotopik kaymanın değerini ve yönünü belirleyin. A. ve B. Dönme seviyesi geçişine karşılık gelen spektral hat için j.. 18. Monotonik olmayan değişikliğin nedenini, molekülün dönüş enerjisindeki en az artışa kadar 19. En büyük göreceli nüfusa karşılık gelen dönme seviyesinin kuantum sayısını belirleyin. Moleküllerin dönme spektrumlarının en yoğun spektral çizgilerinin dalga boylarını hesaplayın A. ve B.. Moleküler spektrumlar yayılma ve emilimin optik spektrumlarının yanı sıra ışığın birleştirilmesinin yanı sıra (bakınız Raman saçılma) ,
serbest veya kötü bağlı molekül m. M. s. Karmaşık bir yapıya sahip olmak. Tipik M. S. - Çizgili, emisyon ve absorpsiyonda ve ultraviyole, görünür ve yakın kızılötesi alanlarda bir dizi veya daha az dar bant şeklinde bir dizi biçiminde saçılması, görülebilir ve yakın kızılötesi alanlarda, kullanılmış spektral cihazların yeterli çözünürlüğünü parçalayın. çizgiler. Özel yapı M. s. Çeşitli moleküller için çeşitli ve genel olarak konuşursak, moleküldeki atom sayısında bir artışla karmaşıktır. Çok karmaşık moleküller için, görünür ve ultraviyole spektrumları birkaç geniş katı şeritten oluşur; Bu tür moleküllerin spektrumları birbirine benzer. h.ν = E.‘ - E.‘’, (1) nerede h.ν, emilen bir fotonun ve frekansın enerjisidir ( h. - Planck sabiti). Kombinasyonel saçılma ile h.ν, olayın enerjilerinin ve dağınık fotonların farkına eşittir. Hanım. Moleküldeki iç hareketlerin daha karmaşıklığı tarafından atomlardan daha fazla karmaşıklığı tarafından belirlenen, dayanıklı atomik spektrumlar tarafından çok daha karmaşıktır. Elektronların moleküllerde iki veya daha fazla çekirdeğe göre hareketi ile birlikte, çekirdeklerin osilatör hareketi (çevreleyen iç elektronlarla birlikte), denge hükümlerinin yakınında ve molekülün bir bütün olarak dönme hareketi yakınında meydana gelir. Bu üç tür hareket - elektronik, salınım ve rotasyonel - üç tür enerji seviyesine ve üç tür spektrumlara karşılık gelir. Kuantum mekaniğine göre, moleküldeki her tür hareketin enerjisi yalnızca belirli değerleri alabilir, yani kuantum. Molekülün tam enerjisi E. Yaklaşık olarak hareketinin üç türünün miktarlaştırılmış enerji değerlerinin toplamı olarak gösterilebilir: E. = E. El +. E. Ülke E. Döndürün. (2) Büyüklük sırasına göre nerede m. - Elektron kütlesi ve değer M. Moleküldeki atomların çekirdeğinin kütlesinin sırasına sahiptir, yani. m / M. Moleküler spektrumlar 10 -3 -10 -5, bu nedenle: E. El \u003e\u003e E. Sayın \u003e\u003e E. Döndürün. (dört) Genelde E. Birkaç sipariş ev (birkaç yüz kJ / MOL),
E. Sayın moleküler spektrumlar 10 -2 -10 -1 eV, E. Rotatörler Moleküler Spektrumlar 10 -5 -10 -3 ev.
(4) uyarınca, molekülün enerji seviyesi sistemi, birbirlerinden uzak bir dizi ile karakterize edilir (çeşitli değerler) E. El pr E. sayım \u003d. E. döndürme \u003d 0), birbirlerine aralıklı salınım seviyelerine çok daha yakın (çeşitli değerler) E. belirtilen ile saymak E. L I. E. Döner \u003d 0) ve daha da yakından dönme seviyeleri (çeşitli değerler) E. Belirtilen ile döndürme E. El I. E. Miktar). Üzerinde İncir. bir
Diatomik molekülün seviyelerinin diyagramı gösterilmiştir; Multiatomik moleküller için seviye sistemi daha da karmaşıktır. Elektronik enerji seviyeleri ( E. (2) ve şemada em İncir. bir
molekülün denge konfigürasyonlarına karşılık gelir (denge değeri ile karakterize edilen iki parçalı bir molekül durumunda) r. 0 İlginç Mesafe r., santimetre. İncir. bir
sanatta. Molekül). Her elektronik durum, belirli bir denge konfigürasyonuna ve belirli bir değere karşılık gelir. E. El; En küçük değer, ana enerji seviyesine karşılık gelir. Molekülün elektronik halleri kümesi elektronik kabuğunun özellikleri ile belirlenir. Prensip olarak, anlam E. El Kuantum Kimya yöntemlerini hesaplayabilir (bkz. Kuantum Kimyası) ,
Ancak, bu görev sadece nispeten basit moleküller için yaklaşık yöntemlerin yardımı ile çözülebilir. Molekülün elektronik seviyeleri (elektronik enerji seviyelerinin düzenlenmesi ve bunların özellikleri), kimyasal yapısı ile belirlenen en önemli bilgiler, M. S ile incelenerek elde edilir. Belirli bir elektronik enerji seviyesinin çok önemli bir özelliği bir kuantum numarasıdır (bkz. Kuantum Numaraları) S, Molekülün tüm elektronlarının tam dönüş anının mutlak değerinin karakterize edilmesi. Kimyasal olarak stabil moleküller, bir kural olarak, bir motorun elektron sayısı ve bunlar için S. \u003d 0, 1, 2 ... (Ana elektronik seviye için tipik olarak S. \u003d 0 ve heyecanlı için - S. \u003d 0 I. S. \u003d 1). Seviye S. S. \u003d 0 singlet olarak adlandırıldı, S. \u003d 1 - üçüz (t. Moleküldeki etkileşim, χ \u003d 2 üzerindeki bölünmelerine yol açar. S. + 1 \u003d 3 Sublevels; Çoklu oyun görmek) .
Serbest radikaller, bir kural olarak, tuhaf elektron sayısı, onlar için S. \u003d 1/2, 3/2, ... ve tipik olarak hem ana hem de heyecanlı seviyeler için S. \u003d 1/2 (χ \u003d 2 takım elbise üzerine bölünmesi). Moleküller için, simetriye sahip denge yapılandırması, elektronik seviyeler daha da sınıflandırılabilir. Diatomik ve doğrusal üçlü moleküller durumunda, tüm atomların çekirdeğinden geçen bir simetri eksenine (sonsuz sipariş) (bkz. İncir. 2.
b) ,
Elektronik seviyeler, molekülün ekseni başına tüm elektronların tamamı yörünge anının yansıtılmasının mutlak değerini belirleyen λ kuantum sayısının değerleri ile karakterize edilir. Λ \u003d 0, 1, 2, ... olan seviyeler, σ, n, δ ... ile gösterilir ve χ değeri yukarıdaki soldaki dizinle gösterilir (örneğin, 3 Σ, 2 π, .. .). Simetri merkezine sahip moleküller için, örneğin CO2 ve C6H6 (bkz. İncir. 2.
, B, b), tüm elektronik seviyeler okuma ve tek endekslere ayrılmıştır. g. ve u (Dalga fonksiyonunun, simetri ortasına ulaşırken veya değiştirirken işaretini durdurup tutarsa \u200b\u200bbağlı olarak). Salınımlı Enerji Seviyeleri (Değerler E. sayım) niceleyin bulunabilir salınım hareketibu yaklaşık olarak harmonik olarak kabul edilir. En basit durumda, boyutsal molekül (bir osilatuar özgürlük derecesi, kesişen mesafedeki değişime karşılık gelen bir salınımsızlık derecesi) r.) Harmonik bir osilatör olarak kabul edilir. ;
Niceleyin, ekibimin enerji seviyeleri verir: E. sayım \u003d. h.ν E (υ +1/2), (5) ν E, molekülün harmonik salınımlarının ana frekansıdır, υ - 0, 1, 2 değer alan bir osilatörlü kuantum numarası, ... üzerinde İncir. bir
İki elektronik devlet için osilatör seviyeleri gösterilmiştir. Oluşan bir multiyomik molekülün her elektronik hali için N. atomlar ( N. ≥ 3) ve sahip olmak f. Salınımsızlık dereceleri ( f. = 3N. - 5 I. f. = 3N. - sırasıyla doğrusal ve doğrusal olmayan moleküller için), ortaya çıkıyor f. t. n. Frekanslı normal salınımlar ν i ( bEN. = 1, 2, 3, ..., f.) ve osilatör seviyelerinin karmaşık sistemi: nerede υ
i \u003d 0, 1, 2, ... - İlgili osilatörlü kuantum numaraları. Normal salınımların frekansları, temel olarak elektronik durumda, kimyasal yapısına bağlı olarak bir molekülün çok önemli bir özelliğidir. Belirli bir normal salınımda, molekülün tüm atomları veya bunların bir kısmı dahil; Aynı zamanda atomlar bir frekansla harmonik salınım yapar v. I, ancak salınım şeklini tanımlayan farklı genliklerle. Normal salınımlar, değerliklerine (iletişim hatlarının uzunluğunun) ve deformasyon üzerindeki şekline göre ayrılır (altında kimyasal bağlar arasındaki açıların). Düşük simetri molekülleri için farklı salınım frekanslarının sayısı (2'nin üzerindeki siparişin bir simetrisi eksenine sahip değildir) 2'dir ve tüm salınımlar dajenere değildir ve daha fazla simetrik moleküller için iki kez ve üç kez dejenere salınımlar (çiftler ve Birlikler salınım sıklığında çakışıyor). Örneğin, doğrusal olmayan bir truch H20 molekülünde ( İncir. 2.
, fakat) f. \u003d 3 ve dejenere olmayan üç salınım mümkündür (iki değerlik ve bir deformasyon). Daha Simetrik Bir Doğrusal Tratment CO 2 Molekülü ( İncir. 2.
b) var f. \u003d 4 - İki nondenerattan salınım (değerlik) ve iki kez dejenere (deformasyon). Düz bir yüksek entegre C6H 6 molekülü için ( İncir. 2.
, c) ortaya çıktı f. \u003d 30 - on nonseenerat ve 10 iki kez dejenere salınım; Bunlardan 14 salınım, molekülün düzleminde (8 değerlik ve 6 deformasyon) ve 6 plazim olmayan deformasyon salınımları - bu düzleme diktir. Daha da daha fazla simetrik tetrahedral molekül CH 4 ( İncir. 2.
, d) var f. =
Şekil 9, dejenere olmayan bir salınım (değerlik), biri iki kez dejenere (deformasyon) ve iki kez dejenere (bir değerlik ve bir deformasyon). Dönme enerji seviyeleri, molekülün dönme hareketini, belirli atalet momentlerine sahip sağlam bir gövde olarak göz önünde bulundurarak (atalet momentine bakınız) olarak görülebilir. İki-paltlanmış veya doğrusal bir multiyotomik molekülün en basit durumunda, dönme enerjisi nerede BEN. - molekülün molekülün eksenine dik eksen'e göre atalet anı ve M. - Hareket miktarının döner anı. Nicelleme kurallarına göre, rotasyonel kuantum numarası J. \u003d 0, 1, 2, ... ve dolayısıyla E. Rotasyonlar var: dönme sabiti nerede İncir. bir Her elektronik salınım durumu için dönme seviyeleri gösterilir. Farklı M. S. Moleküller enerji seviyeleri arasında farklı geçiş türleri vardır. (1) ve (2) 'ye göre Δ E. = E.‘ - E.‘’ = Δ E. El + Δ. E. + Δ say. E. Rotatörler, (8) değiştirildiğinde Δ. E. El, δ. E. Sayı ve δ. E. Elektronik, salınımlı ve dönme enerjisinin dönüşleri durumu karşılar: Δ E. EL \u003e\u003e Δ. E. Saymak \u003e\u003e δ. E. Döndür (9) [aynı siparişin seviyeleri arasındaki mesafeler, enerjilerle E. El, E. OL I. E. Tatmin edici koşullar (4)]. Δ. E. El ≠ 0 Elektronik M. S., Görünür ve ultraviyole (UV) bölgelerinde gözlendi. Genellikle δ. E. El ≠ 0 aynı anda Δ E. Sayım ≠ 0 ve δ E. ≠ 0 döndürün; Çeşitli δ. E. Belirli bir δ ile saymak E. El çeşitli salınım çizgilerine karşılık gelir ( İncir. 3.
) ve farklı δ E. Verildiği gibi döner E. El ve δ. E. Bu şeridin bozulduğu ayrı dönme hatlarının sayısı; Karakteristik çizgili yapı elde edilir ( İncir. dört
). Belirli bir δ ile şeritlerin bir kombinasyonu E. El (frekans ile uygun tamamen elektronik geçiş v. El \u003d δ. E. El / h.) şerit sistemi olarak adlandırılır; Ayrı bantlar, nispi geçiş olasılıklarına (bkz. Kuantum geçişlerine bakınız), yaklaşık olarak kuantum mekanik yöntemlerle hesaplanabilen farklı yoğunluğa sahiptir. Bu elektronik geçişe karşılık gelen bir sistemin karmaşık bant molekülleri için genellikle bir geniş katı şerit halinde birleştirilir, birbirlerini ve birkaç geniş bantları üst üste gelebilirler. Karakteristik ayrık elektronik spektrumlar, organik bileşiklerin dondurulmuş çözeltilerinde gözlenir (bkz. Sposter Etkisi). Elektronik (daha kesin, elektron salınan-dönme) spektrumları, spektrograflar ve camlı spektrometrelerle deneysel olarak incelenir (için görünür alan) ve kuvars (UV bölgesi için), prizmanın veya kırınım katılarının spektrumdaki ışığın ayrıştırmak için kullanıldığı optiklerle (UV bölgesi için) (spektral cihazlara bakınız).
Δ. E. E-posta \u003d 0 ve Δ E. Sayın ≠ 0, osilatör M. S ile elde edilir., Yakın gözlenen (birkaç kadar) μm.) ve ortada (birkaç düzine kadar) μm.) Kızılötesi (IR) alanı, genellikle emilimde olduğu gibi ışığın saçılması. Bir kural olarak, aynı zamanda δ E. ≠ 0 ve belirtildiği gibi döndürün E. Sayı, ayrı dönme hatlarına düşen salınımlı şerittir. Osilatoratuvar M. S'sinde en yoğun. Δ'ye karşılık gelen çizgiler υ
= υ
’ - υ
'' \u003d 1 (multiatomik moleküller için - Δ υ
Ben \u003d. υ
BEN '- υ
i '' \u003d 1'de δ υ
k \u003d. υ
k '- υ
k '' \u003d 0, nerede k. ≠ i). Saf harmonik salınımlar için, bu seçim kuralları ,
yasaklayıcı diğer geçişler kesinlikle gerçekleştirilir; Anmarmonik salınımlar için, bantlar hangi δ υ
\u003e 1 (Aşırı); Yoğunluğu genellikle küçük ve artan δ azalmasıdır. υ
. Osilatoratuvar (daha kesin, salınım-dönme) spektrumları, IR bölgesinde, IR bölgesinde, IR spektrometrelerinin, IR radyasyonu için şeffaf veya difraksiyon ızgaralarının yanı sıra fourier spektrometrelerinin yanı sıra, yüksek- Lazer uyarma kullanımıyla hızlı spektrograflar (görünür alan için). Δ. E. E-posta \u003d 0 ve δ E. Sayım \u003d 0, bireysel çizgilerden oluşan tamamen döner M. s. Uzaktaki absorpsiyonda gözlenirler (yüzlerce yüzlerce) μm.)
IR bölgesi ve özellikle mikrodalga bölgesinde, ayrıca birleşimin saçılma spektrumunda olduğu gibi. Diatomik ve doğrusal poliatomik moleküller için (ve yeterince simetrik olmayan doğrusal olmayan polihidrik moleküller için), bu çizgiler aralıklarla birbirinden (frekans ölçeğinde) eşittir. B. Absorpsiyon spektrumunda ve δν \u003d 4 B. Kombinasyonel saçılma spektrumunda. Saf döner spektrumlar, özel kırınım ızgaraları (eşelatlar) ve Fourier spektrometreleriyle, mikrodalga (mikrodalga) spektrometreler olan mikrodalga alanında, özel kırınım ızgaraları (Achelettes) ve Fourier spektrometrelerine sahip olan uzak bir IR bölgesindeki absorpsiyonda incelenir (bkz. Mikrodalga spektroskopisi) ,
ve ayrıca yüksek hızlı spektrograflarla birlikte saçılma kombinasyonu. Moleküler spektroskopi yöntemleri M. P., Kimya, Biyoloji ve diğer bilimlerin çeşitli görevlerini çözmek mümkündür (örneğin, petrol ürünlerinin, polimerik maddelerin vb. Kompozisyonunu belirlemek için). M. S'ye göre kimyada. Moleküllerin yapısını öğrenin. Elektronik M. S. Moleküllerin elektron kabukları hakkında bilgi edinmek, heyecanlı seviyeleri ve özelliklerini belirlemek, moleküllerin ayrışma enerjilerini bulmak için (molekülün osilatör seviyelerinin ayrılma sınırlarına göre) bulmak için. Osilatoratory M. S tarafından araştırma. Moleküldeki belirli kimyasal bağlara karşılık gelen salınımların karakteristik frekanslarını bulmanızı sağlar (örneğin, basit çift ve üçlü bağlantılar C-C, bağlantılar Sch, N-H, O-H organik moleküller için), çeşitli atom grupları (örneğin, CH2, CH3, NH2), moleküllerin mekansal yapısını belirlemek, BDT ve trans-izomerleri ayırt eder. Bunun için hem kızılötesi emme spektrumları (X) hem de kombinasyonların (ICR) spektrumları kullanılır. Özellikle x yöntemi, moleküllerin yapısını incelemek için en etkili optik yöntemlerden biri olarak yaygınlaştırılmıştır. TCR'nin yöntemi ile birlikte en eksiksiz bilgiyi verir. Dönme M. S., Ayrıca elektronik ve salınımlı spektrumların dönme yapısının yanı sıra, denemeden bulunan moleküllerin moleküllerinin değerlerine, [rotasyonel sabitlerin değerlerinden elde edilen), bkz. 7)] Büyük doğrulukla (daha basit moleküller için, örneğin H20) molekülün denge konfigürasyonunun parametreleri - bağların ve değerlik açılarının uzunluğu. Belirlenen parametrelerin sayısını arttırmak için, izotopik moleküllerin spektrumları incelenmiştir (özellikle hidrojenin deuterium ile değiştirildiği) aynı denge konfigürasyonları parametrelerine sahip, ancak farklı atalet momentlerine sahip. M.S kullanımının bir örneği olarak. Moleküllerin kimyasal yapısını belirlemek için, benzen molekülü C6H6'yı inceleyin. M.'nin çalışması. Molekülün düz olduğuna göre modelin doğruluğunu onaylar ve benzen halkasındaki tüm 6 bağlar C-C eşdeğerdir ve doğru altıgen ( İncir. 2.
B) Altıncı bir sipariş simetri eksenine sahip olmak, uçağına dik molekülün simetri merkezinden geçerek. Elektronik M. S. C6H 6 emme C6H 6, birincisi üçlü ve daha yüksek olan, heyecanlı tek seviyelerdeki ana tek tabanlı tekli seviyesinden geçişlere karşılık gelen birkaç bant sisteminden oluşur. İncir. beş
). 1840 bölgesindeki en yoğun şerit sistemi Å. (E. 5 - E. 1 = 7,0 ev), 3400 bölgede en zayıf sistem şeritleri Å. (E. 2 - E. 1 = 3,8 Ev),
Karşılık gelen tekli-üçlü geçiş, tam dönüş için yaklaşık seçim kuralları ile yasaklanmıştır. Geçişler uyarılmaya karşılık gelir. N. π-elektronlar, benzen halkası boyunca delokalize edilmiş (bkz. Molekül) ;
elektronik moleküler spektrum seviyesinden elde edilen İncir. beş
Yaklaşık kuantum mekanik hesaplamaları ile uyumludur. Osilatoratuvar M. S. C6H 6, simetri merkezinin molekülündeki varlığına karşılık gelir - X'te ortaya çıkan (aktif) salınımların sıklığı (aktif değil) TCR'de (aktif değil) (alternatif yasak). C6H 64'ün 20 normal salınımının, ICR'de aktif olan X ve 7'de aktif olarak aktif hale gelir, kalan 11, hem XA hem de UK'de etkin değil. Ölçülen frekans değerleri (içinde sm -1.):
673, 1038, 1486, 3080 (X) ve 607, 850, 992, 1178, 1596, 3047, 3062 (ICR'de). Frekanslar 673 ve 850 düzlemsel olmayan salınımlara karşılık gelir, diğer tüm frekanslar düz salınımlardır. Özellikle düz salınımların karakteristiği, frekansın (992) (periyodik sıkıştırma ve benzen halkasının gerginliği), frekans 3062 ve 3080 (C - H bağlarının değerlik salınımlarına karşılık gelen) ve frekans 607 () Benzen halkasının deformasyon salınımına karşılık gelir). Gözlenen salınımlı spektrumlar C6H6 (ve salınımlı spektrumlar C6 D 6), bu spektrumların tam bir yorumunu bulmasına izin veren teorik hesaplamalarla çok iyi bir uyum içindedir ve tüm normal salınımların formlarını bulur. Benzer şekilde, M. S ile mümkündür. Örneğin polimer molekülleri, örneğin, çok karmaşık olan organik ve inorganik moleküllerin çeşitli sınıflarının yapısını belirleyin. AYDINLATILMIŞ: Kondratyev V.N., atom ve moleküllerin yapısı, 2 ed., M., 1959; Yeljashevich M. A., Atomik ve Moleküler Spektroskopisi, M., 1962; Herzberg G., Spectra ve diatomik moleküllerin yapısı, per. İngilizce'den M., 1949; Polihidrik moleküllerin, osilatör ve dönme spektrumları, trans. İngilizce'den M., 1949; Elektronik spektrumları ve polihidrik moleküllerin yapısı, başına. İngilizce'den M., 1969; KİMYA, ED'de spektroskopinin kullanımı. V. Vesta, Lane. İngilizce'den M., 1959. M. A. Yeljashevich. İncir. 4. Elektron salınımlı şeridin 3805 Å molekülün n2'sinin döndürülmesi. İncir. 1. Diatomik molekülün enerji seviyelerinin şeması: A ve B - elektronik seviyeleri; v."BEN. v. "- osilatör seviyelerinin kuantum sayıları. J."BEN. J. "- rotasyonel seviyelerin kuantum sayıları. İncir. 2. Denge molekülleri yapılandırmaları: A - H20; B - CO 2; B - C6 H 6; G - CH 4. Sayılar, bağlantıların (å cinsinden) ve değerlik açılarının değerlerini gösterir. İncir. 5. Benzen molekülü için elektronik seviyelerin ve geçişlerin şeması. Enerji seviyeleri verilmiştir ev. C - singlet seviyeleri; T - üçüz seviyesi. Seviye seviyesi G ve U harfleri ile gösterilir. Absorpsiyon bandı sistemleri için, Å'daki örnek dalga boyları belirtilir, bantların daha yoğun sistemleri daha fazla yağ oklarıyla işaretlenir. İncir. 3. Yakın ultraviyole bölgesinde, molekülün elektron salınımlı spektrumu; Grup bantları farklı değerlere karşılık gelir δ v. = v." - v. ". Büyük Sovyet ansiklopedisi. - m.: Sovyet Ansiklopedisi
.
1969-1978
.
Diğer sözlüklerde "moleküler spektrum" olanı izleyin:Serbest veya zayıf bağlantılı moleküllere ait olan ışığın (CRS) emisyon, emilimi ve birleştirilmesi spektrumları. Tipik M. S. Çizgili, UV, görünür ve görülebilir ve ... ..., daha az veya daha az dar bantların birleşimi biçiminde gözlenirler. Fiziksel ansiklopedi Moleküler spektrumlar, emisyon spektrumları, serbest veya kötü ilgili moleküllere ait radyasyonun emilimi ve saçılması. Moleküllerin enerjisinin elektronik, salınımlı ve dönme düzeyleri arasındaki kuantum geçişleri sırasında meydana gelir. ... ... ... Modern ansiklopedi - ELEKTROMAGNET'in emisyon ve emilim spektrumları. Radyasyon ve kombinasyonlar. Serbest veya kötü ilgili moleküllere ait ışığın saçılması. X-ışını, UV, görünür, IR ve Radyo Dalgasında şeritlerin (satır) kombinasyonu biçimlerine sahiptirler (... ... ... Kimyasal Ansiklopediler Spektrum, moleküllerin bazı enerji seviyelerinden başkalarına geçtiğinde ortaya çıkan ışığın optik absorpsiyonu, emisyonu ve kombinasyon saçılmasıdır. Hanım. Az ya da çok geniş çizgili, görüntülerden oluşur. Set yakından bulunur. Spektral ... ... ... Büyük ansiklopedik politeknik sözlük Optik Serbest veya kötü bağlı moleküllere ait emisyon, emilim ve ışığın saçılması spektrumları. Spektral şeritler ve çizgilerden oluşur, ryy'ye yapılan yapı ve yer, yayan moleküller için tipiktir. Kuantum sırasında ortaya çıkar ... ... ... Doğal bilim. ansiklopedik sözlük E-posta spektrumları. MÜRACE. IR'deki radyasyonlar, elektromanyetik dalga terazilerinin görünür ve UV aralıkları. S. Oh. Emisyon spektrumlarına (radyasyon spektrumlarının adı veya emisyon spektrumları), emme spektrumları (emme spektrumları), saçılma ve ... ... Fiziksel ansiklopedi Spectra (optik spektrumlara bakınız) Elektromanyetik dalga terazilerinin kızılötesi, görünür ve ultraviyole aralıklarında elektromanyetik radyasyon (elektromanyetik dalgalar). S. Oh. emisyon spektrumuna bölünmüş (ayrıca spektrum olarak da bilinir ... Büyük Sovyet Ansiklopedisi Molekülün bir bütün olarak döndürülmesinden kaynaklanan moleküler spektrumlar. Kuantum molekülünün dönüşünden bu yana, V. s. Ayrı (neredeyse eşit) çizgilerden oluşur, yani ayrıktır. Vs. uzak bir kızılötesi içinde gözlendi ... ... Big Sovyet Ansiklopedisi, Plikin Vladimir Nikolaevich. Düşük sıcaklık plazma çalışmasının, klasik ve lazer spektroskopi yöntemlerine göre olasılıkları ve mevcut durumu açıklanmaktadır. Sonuçların fiziksel yorumu konuları göz önünde bulundurulur ... Moleküler spektrumlar Serbest veya zayıf bağlantılı moleküllere ait olan ışığın (CRS) emisyon, emilimi ve birleştirilmesi spektrumları. Tipik M. S.-Çizgili, UV, görünür ve IR spektrum bölgelerinde az ya da çok dar bantların bir kombinasyonu biçiminde gözlenir; Spektral cihazların yeterli çözünürlüğü ile diyorlar. Bantlar, yakından yerleştirilmiş çizgilerin bütünlüğüne parçalanır. Yapısı M. s. Bölünme için farklı. Moleküller ve moleküldeki atom sayısında bir artışla karmaşıktır. Çok karmaşık moleküllerin görünür ve UV spektrumları kendi aralarında benzerdir ve birkaç geniş katı şeritten oluşur. Hanım. Enerji seviyeleri arasındaki kuantum geçişleri sırasında ortaya çıkar? "Ve?" Orana göre moleküller: hV, Frekans V'ın yayılan veya emilen fotonun enerjisidir. HV sığırları ile, olayın enerjilerinin ve dağınık fotonların farkına eşittir. Hanım. Daha karmaşıklıkla belirlenen çok daha karmaşık atomik spektrumlar. Moleküldeki hareket, çünkü el-yeni moleküldeki iki veya daha fazla çekirdeğin hareketi yanı sıra, salınımlar meydana gelir. Çekirdeğin hareketi (çevreleriyle birlikte. Al-ABD) dengenin konumuna yakın ve döndürün. Bir bütün olarak hareket ettirin. Elektronik, OSCIL. Ve döndürün. Molekülün hareketleri üç tür enerji seviyesine karşılık gelir mi? El,? Pumber ve? BB H Üç tip M. s. Kuantum'a göre. Mekanik, moleküldeki her tür hareketin enerjisi yalnızca belirli değerleri (kuantum) alabilir. Komple Enerji Molekülü? Üç türünün üç türüne karşılık gelen enerjilerin miktarlaştırılmış değerlerinin toplamı olarak yaklaşık olarak temsil edilebilir. Hareketler: ? "? El +? Count +? BP, (2) ve büyüklük sırasına göre El :? Sayım :? BP \u003d 1: M / M: M / M, (3) n, e-posta kitlesidir ve M, moleküldeki atomların çekirdeğinin kütlesinin emrine sahiptir. El -\u003e? Count -\u003e? Bp. (4) Genellikle? EV (yüzlerce kj / mol),? Count \u003d 10-2-10-1 EV,? BP \u003d 10-5-10-3 EV. Molekülün enerji seviyeleri sistemi, elektronik enerji seviyelerinin agregaları ile birbirinden uzakta (bölünmüş. EL? COUNT \u003d? BP \u003d 0). Salınım seviyelerinin birbirlerine önemli ölçüde daha yakın bulunur (split. Belirli bir e-posta ve? Vp \u003d 0 için muhasebeleştirilir? VP \u003d 0) ve hatta dönme seviyeleri (değerler? BP ile belirtilenler? Ele ve? Sayım) ile birbirine daha yakın. Elektronik enerji seviyeleri Şekil 2'de bir K B. 1 denge molekül konfigürasyonlarına karşılık gelir. Her elektronik durum, kesin bir denge konfigürasyonuna ve belirli bir değere karşılık gelir mi? En küçük değer ana'ye karşılık gelir. Elektronik Devlet (OSN. Elektronik molekül enerjisi). İncir. 1. Diatomik molekülün, A ve B elektronik seviyelerinin enerji seviyelerinin şeması; V "ve v" - Kvant. Sayılar. Seviyeler; J "ve j" - Kvant. Sayılar döner. seviyeleri. Molekülün elektronik halleri kümesi elektronik kabuğu ile belirlenir. Prensip olarak, değeri? El Kuantum yöntemlerini hesaplayabilir. Bununla birlikte, kimya, bu görev sadece nispeten basit moleküller için çözülür. Kimyasal tarafından belirlenen elektronik moleküllerin (konumu ve harekeleri) seviyeleri hakkında önemli bilgiler. Yapı, M. s çalışarak elde edilir. Son derece önemli Har-KA elektronik enerji seviyesi, ABS'yi tanımlayan bir kuantum 5'in değeridir. Tüm EL-New'in tam dönüş anının büyüklüğü. Kimyasal olarak kararlı moleküller, bir kural olarak, e-posta sayısı ve bunlar için 5 \u003d 0, 1, 2,. . ; Arazi için. Elektronik seviye tipik olarak 5 \u003d 0, heyecanlı - 5 \u003d 0 ve 5 \u003d 1 içindir. S \u003d 0 ile seviye denir. S \u003d 1 - üçüzü ile singletny (Muulilikleri C \u003d 2S + 1 \u003d 3). Diatomik ve doğrusal trotham molekülleri durumunda, elektronik seviyeler kuantum değeri ile karakterize edilir. Abs tanımlayan sayılar. Molekülün ekseninde tüm EL-YENİ'nin tamamı yörünge anının ortaya çıkmasının büyüklüğü. L \u003d 0, 1, 2 olan seviyeler, sırasıyla S, P, D,. . ., A ve yukarıdaki soldaki dizinle gösterilir (örneğin, 3S, 2P). Simetri merkezine (örneğin, CO2, CH6) sahip olan moleküller için, tüm elektronik seviyeleri, simetri merkeziyle iletişime geçerken, dalga işlevlerini tanımlayanlara bağlı olarak, okuma ve tek (G ve U, sırasıyla) ayrılır. Salınımsal enerji seviyeleri, salınımların ölçülmesini sağlayabilir. Yaklaşık yaklaşık harmonik olarak kabul edilen hareket. Çift soğutmalı molekül (bir salınım. İnterstisyel mesafedeki değişime karşılık gelen özgürlük derecesi) harmonik olarak kabul edilebilir. Osilatör, Quino'nun nicelemesi eşit derecede enerji verir: nerede v - osn. Frekans harmonik. Molekülün salınımları, V \u003d 0, 1, 2,. . .- Osilatörler. kuantum. numara. N 3 atomundan oluşan ve funilasyonlardan oluşan bir multiyomik molekülün elektronik hali için. Özgürlük dereceleri (F \u003d 3N-5 ve F \u003d 3N-6, sırasıyla doğrusal ve doğrusal olmayan moleküller için), yanar / t. Frekanslı normal salınımlar VI (hasta, 2, 3, ..., f) ve karmaşık bir salınım sistemi. Enerji seviyeleri: Normların frekansları kümesi. OSN'de salınımlar. elektronik hali. Kimyasalına bağlı olarak önemli bir harekal molekül. Binalar. Belirli bir norm içinde. Salınımlar, molekülün tüm atomlarını veya bir kısmının; Atomlar harmonik yapar. Aynı frekans vi ile salınımlar, ancak bölünmüş. Salınım şeklini tanımlayan genlikler. Norm. Salınımlar, değere (kimyasal bağların uzunlukları) ve deformasyon üzerine (kimyasal bağlar arasındaki açılar değiştirilir) şeklinde ayrılır. En düşük simetri molekülleri için (molekülün simetrisine bakınız) F \u003d 2 ve tüm salınımlar nondenerater; Daha fazla simetrik molekül için, iki kez ve üç kez dejenere salınımları, yani, çiftler ve üç kez salınım sıklığında çakışır. Enerjinin dönme seviyeleri niceleyin döndürülebilir. Molekülün hareketi, TV olarak göz önüne alındığında. Tanımlanmış anlar ataletli gövde. Diatomik veya doğrusal bir trakan molekülü durumunda, dönme enerjisi? BP \u003d M2 / 2I, burada ben molekülün eksenine dik eksene göre molekülün atalet momentidir ve m - döndürün. Hareket sayısının anı. Nicelleme kurallarına göre, M2 \u003d (H / 4PI2) J (J + 1), burada f \u003d 0, 1,2,. . .- Rotasyonel Kuantum. numara; İçin? Biz alıyoruz: BP \u003d (H2 / 8PI2I) J (J + 1) \u003d HBJ (J + 1), (7) nerede döner. Kalıcı \u003d (H / 8PII2) I enerji seviyeleri arasındaki mesafelerin ölçeğini belirler, çekirdeklerin kütlelerindeki artış ve interstarrial mesafelerin artması ile azalır. Bölünmüş. M. s türleri. ne zaman ortaya çıkıyor Moleküllerin enerji seviyeleri arasındaki geçiş türleri. (1) ve (2) göre: D? \u003d? "-?" \u003d\u003d D? El + D? Count + D? BP, ve benzer şekilde, (4) D? El-\u003e d? Count-\u003e D? BP. Ne zaman D EL? 0, Elektronik M. S., Görünür ve UV bölgelerinde gözlendi. Genellikle d ?? 0 aynı zamanda d? Sayısı? 0 ve D? BP? 0; Bölünmüş. D? Belirli bir D? EL ile Pake Ring'e karşılık gelir. OSCIL. Şeritler (Şekil 2) ve bölünmüş. D? BP Verilen D? El ve D? Sayısı döndürün. Çizgiler, salınımların parçalandığı. Şeritler (Şek. 3).  İncir. 2. Elektrik salınımı. Yakın UV bölgesindeki N2 molekülünün spektrumu; Grup bantları halka'ya karşılık gelir. Değerler DV \u003d V "-V". Belirli bir D? EL içeren bir grup bant (nal \u003d D? E / H sıklığı ile tamamen elektronik bir geçişe karşılık gelen) denilen. sistem şeritleri; Şeritlerin bir dönüşü var. aşağıdakilere bağlı olarak yoğunluğu. Geçiş olasılıkları (bir kuantum geçişine bakınız).  İncir. 3. Döndür. Elektron-Cingbat bölünmesi. Çizgiler 3805.0? Moleküller n2. Bu elektronik geçişe karşılık gelen bir sistemin şeridinin karmaşık molekülleri için genellikle bir geniş katı şerit halinde birleştirilir; birbirlerine ve birkaç üzerinde örtüşebilir. Böyle şeritler. FROZEN R-RAF organik olarak karakteristik ayrık elektronik spektrum görülür. Bağlantılar. Elektronik (daha kesin, elektron salınımlı) spektrumlar, cam (görünür bölge) ve kuvars (UV bölgesi, (ultraviyole radyasyonu)) optiği olan spektral cihazlar kullanılarak incelenmiştir. Ne zaman D? EL \u003d 0 ve D? SAYI? 0 0 açılır. M. S., Yakın IR bölgesinde, genellikle emilim ve sığır spektrumlarında gözlendi. Kural olarak, verilen bir D? COUNT D? BP? 0 ve salınımlar. Şerit kapalıyken parçalanır. döndürün. çizgiler. Salınımlara en yoğun. Hanım. DV \u003d V "- V" koşulunu tatmin eden şeritler (multiatomik moleküller için DVI \u003d V "i- V" i \u003d 1 DVK \u003d v "KV" K \u003d 0; burada I ve K milini belirler. Normal dalgalanmalar ). Tamamen harmonik için. Salınımlar Bu seçim kuralları kesinlikle gerçekleştirilir; Anharmonik için. Salınımlar, RY DV\u003e 1 (aşırı yük) için çizgilidir; Yoğunluğu genellikle küçüktür ve DV'deki artışla azalır. OSCIL. Hanım. (Daha kesin olarak, osilasyon-dönüş), IR spektrometreleri ve Fourier spektrometreleri ve sığırların spektrumları kullanılarak çalışılır - Lazer uyarma kullanımı ile hafif spektrograflar (görünür bölge için). D "EL \u003d 0 ve D? COUNT \u003d 0, tamamen döndürülürken elde edilir. Mevduattan oluşan spektrumlar. çizgiler. Uzak bir IR bölgesindeki emme spektrumunda ve özellikle mikrodalga bölgesinde ve ayrıca sığırların spektrumundaki gözlenirler. Diatomik, doğrusal trotham molekülleri ve yeterince simetrik olmayan doğrusal olmayan moleküller için, bunlar birbirinden (frekans ölçeğinde) eşittir. Tamamen döndürün. Hanım. Özel ile IR spektrometrelerini kullanarak öğrenin. Diffrakts. Kafesler (Achelertes), Fourier spektrometreleri, ters dalga lamba, mikrodalga (mikrodalga) spektrometrelere dayanan spektrometreler (bkz. Submillimeter spektroskopisi, mikrodalga spektroskopisi) ve döndürün. CRS spektrumları - hafif spektrometre ile. Moleküler spektroskopi yöntemleri M. P., Çeşitli kimya görevlerine izin verir. Elektronik M. S. Elektronik kabukları, heyecanlı enerji seviyeleri ve Hark-Kakları, moleküllerin ayrışma enerjisi ile ilgili bilgi sağlarlar (ayrışma sınırına göre amaçlanan enerji seviyesi ile). Çalışma salınımı. Spektrumlar, belirli kimyasal türlerinin molekülündeki varlığına karşılık gelen salınımların karakteristik frekanslarını bulmanızı sağlar. İlişkiler (örneğin, çift ve üçlü bağlar C-C, organik için C, N-N bağlantıları), boşlukları belirlemek için. Yapı, BDT ve trans izomerleri arasında ayrım yapar (bkz. Moleküllerin izomerizmi). Özellikle kızılötesi spektroskopinin yaygın yöntemleri - en etkili optiklerden biri. Moleküllerin yapısını incelemek için yöntemler. Bunlar, SCR spektroskopisinin yöntemleri ile birlikte en eksiksiz bilgidir. Çalışma döner. Spektrumların yanı sıra döndürün. Elektronik ve salınım yapıları. Hanım. Moleküller ataletini moleküllerin deneyiminden büyük bir doğrulukla bulmanıza olanak sağlar, denge konfigürasyonlarının parametreleri, tahvillerin ve değerlik açılarının uzunluklarıdır. Belirlenen parametrelerin sayısını artırmak için, izotop spektrumları incelenmiştir. Moleküller (özellikle, yeniden hidrojendeki moleküller, deuterium ile değiştirilir), aynı denge konfigürasyonlarının aynı parametrelerine sahip, ancak ayrılır. Anlar Ataları. Hanım. BA'nın bileşimini belirlemek için spektral analizde de uygulanır.
Moleküler spektrumların çalışmaları, moleküldeki atomlar arasında hareket eden kuvvetleri, molekülün ayrışma enerjisi, geometrisi, özdeş mesafeleri vb. . Molekülün yapısı ve özellikleri hakkında geniş bilgi verin. Moleküler spektrumun altında, geniş bir anlamda, geçiş enerjisine bağlı olarak molekülün (bkz. 9) arasındaki bireysel iki enerji seviyesi arasındaki geçiş olasılığının dağılımı olarak anlaşılmaktadır. Gelecekte Optik Spectra hakkında olacağından, bu bir geçişin her bir geçişin enerji ile foton yayan veya emici olması ile eşlik etmelidir. E n \u003d hn \u003d e 2 - e 1, 3.1 burada e 2 ve e 1 - geçişin gerçekleştiği enerji seviyeleri. Gaz molekülleri tarafından yayılan fotonlardan oluşan radyasyon, spektral cihazdan geçer, daha sonra ayrı parlak (renk olabilir) çizgilerden oluşan molekülün emisyon spektrumu. Ayrıca, her satır karşılık gelen geçişe karşılık gelecektir. Buna karşılık, yelpazedeki çizginin parlaklığı ve konumu, sırasıyla geçiş ve enerji (frekans, dalga boyu) foton olasılığına bağlıdır. Aksine, bu gazdan ve ardından tüm dalga boylarının fotonlarından (katı spektrum) oluşan radyasyonu atlamak için spektral cihazdan sonra, emme spektrumu elde edilir. Aynı zamanda, bu spektrum, parlak bir katı spektrumun arka planında bir dizi koyu çizgiler olacaktır. Buradaki spektrumdaki hattın kontrastı ve konumu, geçiş ve foton enerjisinin olasılığına da bağlıdır. Molekülün enerji seviyelerinin karmaşık yapısına dayanarak (bkz. Şekil 9), bunlar arasındaki tüm geçişler, moleküllerin spektrumunun farklı bir karakterini veren ayrı tiplere ayrılabilir. Molekülün salınımlı ve elektron halini değiştirmeden dönme seviyeleri (bkz. Şekil 8) arasındaki karşılık gelen geçişlerden oluşan spektrum, molekülün dönme spektrumu denir. Dönme hareketinin enerjisi 10 -3 -10 -5 EV içinde yattığından, bu spektrumdaki çizgilerin frekansı, radyo frekansının (uzak kızılötesi alan) mikrodalga bölgesinde yatmalıdır. Aynı elektronik durumdaki molekülün farklı salınım durumlarına ait dönme seviyeleri arasındaki karşılık gelen geçişlerin çizgilerinden oluşan spektrum, molekülün titreşimi ve dönme veya basit salınımlı spektrumu denir. Bu spektrumlar, salınım hareketinin 10 -1 -10 -2 EV'nin enerjilerinde, frekansın kızılötesi bölgesinde uzanır. Son olarak, molekülün farklı elektronik ve salınımlı durumlarına ait dönme seviyeleri arasındaki karşılık gelen geçişlerin çizgilerinden oluşan spektrum, molekülün elektron salınımlı-rotasyonel veya sadece elektron spektrumu olarak adlandırılır. Bu spektrumlar, sıklığın görünür ve ultraviyole bölgelerinde yatıyor, çünkü Elektronik hareket enerjisi biraz elektrondur. Foton emisyonu (veya emilim) bir elektromanyetik işlem olduğundan, o zaman Önkoşul Moleküldeki karşılık gelen kuantum geçişi ile ilişkili elektrik dipol anındaki değişim veya daha kesin olarak. Dönme ve salınımlı spektrumun sadece elektrik dipol anı olan moleküllerde gözlenebileceğini takip eder. heterojen atomlardan oluşan. Moleküler spektrumlar, emisyon spektrumları ve elektromıknatıs emilimi. Radyasyon ve kombinasyonlar. Serbest veya kötü ilgili moleküllere ait ışığın saçılması. X-ışını, UV, görünür, IR ve radyo dalgası (mikrodalga) spektrumundaki (mikrodalga) bölgelerinde bir dizi grup (satır) formlarına sahiptirler. Şeritlerin (satırların) emisyon spektrumundaki (emisyon moleküler spektrumları) ve absorpsiyon (emme moleküler spektrumları) konumu, frekanslar V (Wavelents L \u003d C / V, burada C-Hızının) ve dalga sayıları \u003d 1 ile karakterizedir. / l; EN "ve E'sinin farkı ile belirlenir. Ve E: Molekülünkiler, k-fish arasında bir kuantum geçişi meydana gelir:
(H-Constant Planck). Bir kombinatör ile. Saçılma HV'nin değerini, olayların enerjilerinin farkına eşittir ve dağınık fotonlardır. Şeritlerin (satırların) yoğunluğu, bu türün moleküllerinin sayısı, E "ve e'sinin popülasyonunu, ve e: ve karşılık gelen geçişin olasılığı ile ilişkilidir. Radyasyonun emisyonu veya emilimine sahip geçişlerin olasılığı, öncelikle elektronun matris elemanının karesi ile belirlenir. Geçişin dipol anı ve daha doğru bir şekilde göz önünde bulundurularak - ve matris elemanlarının kareleri. ve elektrik. molekülün dörtlü anları (bkz. Kuantum geçişleri). Bir kombinatör ile. Işık saçılması Geçiş olasılığı, molekülün geçişinin indüklenen (indüklenmiş) dipol anının matris elemanı ile ilişkilidir, yani. Molekülün polarizarlığının bir matris elemanı ile. Koşullar mol. Sistemler, K-Balığı arasındaki geçişler, belirli bir moleküler spektrum biçiminde tezahür edilir, farklı doğaya sahip ve enerji ile büyük ölçüde farklılık gösterir. Bazı türlerin enerji seviyeleri birbirinden uzak bulunur, böylece molekül geçişleri, yüksek frekanslı radyasyon emer veya yayılır. Diğer doğanın seviyeleri arasındaki mesafe yeterli değildir ve bazı durumlarda dışın yokluğunda. Seviye alanları birleştirme (dejenere). Düşük farklılıklarla, geçişler düşük frekanslı bir alanda gözlenir. Örneğin, bazı unsurların atomlarının çekirdeği kendilerine sahiptir. MÜRACE. An ve elektrik. Döndürme ile ilişkili bir dörtlü nokta. Elektronların da mantarları var. Sırtları ile ilişkili an. Dışın yokluğunda Oryantasyon alanları. MESAK ANTILARI, yani. Sakla olmazlar ve karşılık gelen enerji. Devletler dejenere. Dış uygulandığında. kalıcı olarak. Alanlar dejenerasyondan çıkarılır ve spektrumun radyo frekans bölgesinde gözlenen enerji seviyeleri arasındaki geçişler mümkündür. Böylece NMR ve EPR spektrumları vardır (bkz. Nükleer manyetik rezonans, elektronik paramanyetik rezonans). Kinetich tarafından dağıtım. Mol tarafından yayılan elektron enerjileri. X-ışını veya sert UV radyasyonu olan radyasyon sonucu sistemler, X-rayemctron veriyorspektroskopi ve fotoelektron spektroskopisi. Tamamlayınız Köstebek süreçleri. İlk uyarma neden olduğu sistem, diğer spektrumların görünümüne yol açar. Böylece, spektrumlar gevşeme sonucu ortaya çıkıyor. Dış ile elektron yakalama. Shell K.L. İçinde boşta atom. Kabuk ve serbest bırakılan enerji dönüyor. Kinetich'te. Enerji DR. Elektron Dış Atomun yaydığı kabuk. Aynı zamanda, nötr bir molekülün köstebek durumuna belirli bir durumdan kuantum geçişi gerçekleştirilir. İyon (bakınız burgu spektroskopisi). Geleneksel olarak, sadece optik ile ilişkili spektrumlar moleküler spektrumları içerir. Elektron salınması arasındaki geçişler döndürülür, üç AUDN ile ilişkili molekülün enerji seviyeleri. Enerji türleri. Molekülün seviyeleri - elektronik ∈ EL, salınım e, üç tür dahili karşılık gelen rotasyonel e bp. Moleküldeki hareket. E-e-posta, bu elektronik durumda molekülün denge yapılandırmasının enerjisini alır. Molekülün olası elektronik hallerinin bir dizi elektronik kabuğu ve simetrisi ile belirlenir. OSCIL. Çekirdeğin molekülündeki tüm elektronik durumdaki denge konumlarına ilişkin hareketleri, birkaç salınımla ölçülür. Özgürlük dereceleri, karmaşık bir salınım sistemi oluşturur. Enerji seviyeleri E sayısı. Molekülün bir bütün olarak birbirine sahip çekirdekli bir sistem sistemi olarak dönmesi, rotat karakterizedir. Bir kuantum olan hareket sayısının anı, döndürme oluşturur. Devletler (döndürme. Enerji seviyeleri) E BP. Genellikle, çeşitli siparişin elektronik geçişlerinin enerjisi. EV, Osilatory-10 -2 ... 10 -1 EV, Rotational-10 -5 ... 10 -3 EV. Emisyonlu geçişlerin, emme veya kombinasyonların hangi enerji seviyelerinin arasında meydana gelmemesine bağlı olarak. Saçılma Electomagnet. Radyasyon - Elektronik, salınımlar. veya dönme, elektronik ayırt eder, salınımlar. ve dönme moleküler spektrumları. Makalelerde, elektronik spektrumlar, salınımlı spektrumlar, dönme spektrumları, karşılık gelen moleküller, kuantum geçişleri için seçim kuralları, Mol yöntemleri hakkında bilgi verilir. Spektroskopi, ayrıca moleküllerin özellikleri hakkında. b. b. Moleküler spektrumdan elde edilen: SV-VA ve elektronik devletlerin simetrisi, salınır. Kalıcı, ayrışma enerjisi, molekülün simetrisi, döndürür. Kalıcı, atalet anları, geom. Parametreler, elektrik. Dipoller, yapı ve iç veriler. Elektrik alanları, vb. Görülebilir ve UV bölgelerinde elektronik emilim ve lüminesans spektrumları dağıtım hakkında bilgi verir. |
Popüler:
Yeni
- Tag: Birkaç değişkenin fonksiyonları İki değişkenin diferansiyelinin geometrik anlamı
- Teorem, teoremin dinamiğinin hareket sayısındaki hareket üzerindeki hareket miktarı
- Teoremin dinamiklerinin mekanik sisteminin miktarını değiştirme, hareket miktarındaki değişimde
- Serbest düşme hızı
- Farklı analiz kullanmadan fonksiyonların sınırlarını nasıl hesaplanır?
- Degrade Fonksiyonu Nasıl Bulunur?
- Noktadan Noktadan Uzaklık: Formüller, Örnekler, Çözümler
- Detaylı bir kararla her türlü sınırın çözümü
- Kesitli atalet anları
- Nokta ile düzlem, direkt ve düzlem arasındaki mesafenin, uçaklar ve çapraz yaşadığı düzlük arasındaki mesafeyi belirleme

 .
.
 - yüksek ve daha düşük seviyelerde elektron enerjileri; -
- yüksek ve daha düşük seviyelerde elektron enerjileri; -  - Dalga sayılarının ölçülmesi birimlerinde ifade edilen spektral terimler (M -1, cm-1).
- Dalga sayılarının ölçülmesi birimlerinde ifade edilen spektral terimler (M -1, cm-1).
 =25,9 kJ / Mole
=25,9 kJ / Mole =3,8 kJ / Mol.
=3,8 kJ / Mol.
 - Elektronik Seviyeler;
- Elektronik Seviyeler;
 .
.
 .
.

 .
.
 20
20  12
12 
 ,
,
 . Değişiklik sadece çok büyük bir şekilde dikkate alınmalıdır. j..
. Değişiklik sadece çok büyük bir şekilde dikkate alınmalıdır. j.. . Moleküldeki simetri elemanlarının varlığında, ataletin anları çakışabilir, hatta sıfır olabilir. Örneğin, doğrusal poliatomik moleküller için (CO 2, OCS, HCN, vb.)
. Moleküldeki simetri elemanlarının varlığında, ataletin anları çakışabilir, hatta sıfır olabilir. Örneğin, doğrusal poliatomik moleküller için (CO 2, OCS, HCN, vb.) - Çizginin dönme geçişine karşılık gelen konumu
- Çizginin dönme geçişine karşılık gelen konumu  İzotopianlaştırılmış bir molekülde.
İzotopianlaştırılmış bir molekülde. Dalga sayılarının oranı, ortaya çıkan kütlelerin zıt oranına karşılık gelir:
Dalga sayılarının oranı, ortaya çıkan kütlelerin zıt oranına karşılık gelir: ,
,
 - İstatistiksel Ağırlık j.Enerjinin dönme seviyesi, ekseni üzerindeki dönen molekül miktarının projeksiyonlarının sayısına karşılık gelir - molekül iletişim hattı,
- İstatistiksel Ağırlık j.Enerjinin dönme seviyesi, ekseni üzerindeki dönen molekül miktarının projeksiyonlarının sayısına karşılık gelir - molekül iletişim hattı,  , sıfır dönme seviyesinin enerjisi
, sıfır dönme seviyesinin enerjisi  . İşlev artarken maksimum geçer j.CO molekülü örneğinde Şekil 4.7'de gösterildiği gibi.
. İşlev artarken maksimum geçer j.CO molekülü örneğinde Şekil 4.7'de gösterildiği gibi. .
.


 sm -1.. Dönme sabitini, atalet momentini ve moleküldeki denge interstisyel mesafesini hesaplayın.
sm -1.. Dönme sabitini, atalet momentini ve moleküldeki denge interstisyel mesafesini hesaplayın. sm -1..
sm -1.. kilogram . m 2..
kilogram . m 2.. ve iyot
ve iyot  kg'da ifade edilir:
kg'da ifade edilir: Sm -1.
Sm -1. ve klor
ve klor  (kg'da ifade edilir):
(kg'da ifade edilir):
 Enerji seviyesi, 37 CL izotop üzerindeki klorin atomunu değiştirirken, 1H35 C molekülün dönme spektrumunda. 1 saat 35 molekül 1 H 37 fıkrasında bir interstisyel mesafe aynıdır.
Enerji seviyesi, 37 CL izotop üzerindeki klorin atomunu değiştirirken, 1H35 C molekülün dönme spektrumunda. 1 saat 35 molekül 1 H 37 fıkrasında bir interstisyel mesafe aynıdır. 1H37 molekülünün spektrumunda, izotopun denklemlerle (4.35), (4.39), (4.43) ve (4.50), sırasıyla değişimin büyüklüğü.
1H37 molekülünün spektrumunda, izotopun denklemlerle (4.35), (4.39), (4.43) ve (4.50), sırasıyla değişimin büyüklüğü.
 Denklemde CM -1) (4.54), bu enerji seviyesinin sayısını hesaplamanızı sağlar:
Denklemde CM -1) (4.54), bu enerji seviyesinin sayısını hesaplamanızı sağlar: .
. .
.